叶定伟教授:前列腺癌雄激素剥夺治疗的副作用——不可忽视的另一面
随着人口老龄化和生活方式的西化,前列腺癌已经成为危害中国男性健康的高发病率恶性肿瘤。雄激素剥夺治疗(androgen deprivation therapy,ADT),包括采用药物或手术降低体内雄激素水平,是前列腺癌综合治疗中的重要一环。
在转移性前列腺癌患者中,ADT是标准治疗方案,有效时间约为3年,即使在肿瘤进展为去势抵抗期仍然需要维持睪酮在去势水平。在局部晚期或高危前列腺癌患者中,ADT作为重要的组成部分能显著改善肿瘤控制和长期生存率。在初始治疗后复发或无症状的局限性前列腺癌患者中,ADT的介入时机和风险获益比还存在争议,然而在临床实践中的应用却相当广泛。当我们面对高龄、众多并发病、长疗程治疗的前列腺癌患者人群时,系统全面的认识ADT的副作用具有重要意义。本文回顾近年来发表的相关文献,概述副作用的种类、发生率和应对策略,有助于ADT过程中的精细化患者管理。
ADT会在一个月之内将血清睪酮水平迅速降低至50ng/dl,接近原来的1/10。剧烈的雄激素波动随之而来产生一系列复杂的身心改变,造成全身多系统的失衡,长期的不良后果不容忽视,本文将归纳为四个方面加以阐述:生活质量;骨骼健康;心血管健康;新型内分泌治疗的副作用。
一、生活质量
(一)认知、情绪与抑郁
接受ADT的往往是初诊的晚期前列腺癌患者,雄激素水平的变化会进一步加重患者的心理打击。在一项关于新诊断转移性前列腺癌的调研中,将近三分之一的患者被认为是精神高度压抑的,同时在12个月内这一人数还在增加。自杀风险也相对于同龄人群的对照组增加了4倍[1]。而且,ADT被认为还会损害记忆力、注意力以及决策功能。在一项随机对照试验中,Green等人发现在6个月的ADT后,将近半数的患者出现了明显的认知能力(包括注意力以及记忆力)的下降[2]。因此,对那些不需要即刻ADT的患者,可以允许他们先有一段时间的心理调整。这会给患者以及其家庭提供足够的时间来了解疾病、相关治疗以及他们该作出怎样的决策。不仅如此,心理社会学上的介入比如前列腺癌科普教育、咨询心理治疗师以及病患交流群也有助于提升患者的总满意度以及生存质量。
(二)性欲降低、性功能障碍与生殖器缩小
性功能障碍是影响患者生存质量和自我认知的重要因素[3]。根据报告,性欲降低的发病率从58%~91.4%,勃起功能障碍的发病率自73.3%~95%不等,同时93%的人发现阴茎长度的缩小程度大于1cm[4]。勃起功能障碍可以采用药物治疗——PDE抑制剂和海绵体内注射,也可以采用真空负压吸引设备或阴茎假体植入。
(三)男子乳房发育与乳腺痛
男子乳房发育定义为乳晕下腺体以及导管组织的增生,同时可能会伴有乳腺疼痛。LHRHa治疗后约有30%的患者出现乳腺不适,抗雄药物(如比卡鲁胺)导致男子乳房发育以及乳腺痛的发生率可高达90% [4]。针对乳腺腺体的放疗或预防性使用他莫昔芬可以有效地减少此类不良反应的发生,然而在临床上更常用的是采用镇痛药物对症缓解症状[5]。
(四)潮热
潮热是最常见的ADT副作用,接近80%的患者主诉有突然出汗以及面部发红的不适感[4]。某些人可能会产生虚脱的感觉,甚至导致患者拒绝接受ADT。在生活方式上,可以尽量回避引发潮热的刺激因素,如咖啡因、辛辣和滚烫的食物。一些药物也可以用于治疗潮热。在随机对照试验中,文拉法辛(SSRI,75mg),醋酸环丙孕酮(100mg)以及醋酸甲羟孕酮(20mg)都可以在服用一个月后缓解潮热症状(症状评分的减轻程度分别为:47.2%,94.5% 和 83.7%)[6]。值得一提的是,应用醋酸环丙孕酮前需要了解并评估其诱发骨质疏松、乳腺发育和肥胖的副作用。
(五)体能状况
雄激素水平降低可以加速肌肉萎缩从而引起体能状况的恶化,运动疗法可以刺激多器官的生理性改变,有助于缓解ADT引起的副作用。Galvao和Nweton提出了“监督下锻炼方案”这一概念,并作为ADT治疗中的重要组成部分。在近期的一项随机对照研究中,在ADT的早期进行运动疗法敢于可以保证体重恒定、减少身体脂肪含量、增加骨密度、维持胆固醇水平稳定[7]。这和非运动干预的对照组中发生肥胖、骨密度丢失、脂代谢异常以及肌肉萎缩一系列现象等形成鲜明对比。而且,生理功能以及生活质量包括性功能、疲劳以及精神压力这些指标都得到了明显的改善。
然而,如果在ADT后几个月甚至几年后再对患者开始进行运动干预,结果就没有那么显著。TTROG试验显示:虽然锻炼可以提升身体健康程度、生理功能、肌肉强度以及心理健康,但是获益的程度却不如那些在ADT之初便给予运动疗法的患者[8]。Gardener的meta分析提示:尽管随机对照试验有着不一样的结果,但患者接受运动疗法还是有明显的临床获益。“监督下锻炼方案”的维持时间可以延续到后半年以上,因此建议体力情况尚可的患者每天进行30分钟的中等强度运动[9]。
二、骨骼健康
在诊断为前列腺癌时,老年男性罹患骨质缺乏以及骨质酥松的概率高达39%与41% [10]。在ADT的第一年,骨密度丢失的绝对值约为5% [11,12]。在ADT后4年与10年时骨质疏松的发生率可分别达到49.2%与80.6%。由于在骨骼实际密度降低的基础上,骨小梁数也在减少,因此常规骨密度检查往往低估了骨质疏松的程度。骨密度降低增加骨折风险,而骨折风险与前列腺癌患者的死亡率密切相关。在大型的观察性研究中,ADT将骨折风险增加34%,并且骨折发生后患者死亡率将翻增。
双磷酸盐可以将降低破骨细胞的活力从而减少了骨密度丢失。每周口服阿仑膦酸钠可以在非转移性前列腺癌患者中维持骨密度的稳定。静脉注射的唑来膦酸药效更强,长期应用可以将骨密度提升4% [13]。然而,尽管骨密度得以提高,但是上述治疗没有减少骨折发生的概率或者增加总生存率,也没有延缓骨转移发生的时间。对于去势抵抗性前列腺癌,静脉给予双膦酸盐可以可以减少骨折发生的风险。当药物应用剂量较高时,需要注意破坏性的药物反应,比如低钙血症、下颌骨坏死,需要进行治疗前的评估以及随访。
Denosumab是一种针对RANK配体的单克隆抗体,RANK配体是调控破骨细胞功能与增殖的关键因子。抑制这个配体可以阻止骨骼的吸收以及破骨细胞的存活。现有研究发现,在非转移性前列腺癌患者中,每半年给予60mg的Denosumab,持续24个月,可有增加骨密度(5.6%与1%)以及减少骨折概率(1.5% 与 3.9%)的作用[14]。高剂量短间隔的使用(120mg,每4周1次)可以延缓CRPC患者中骨骼相关事件的发生时间(3.6个月),以及骨转移的发生时间(4.2个月)。和双磷酸盐相似,Denosumab也与低钙血症(2%)与下颌骨坏死(5%)有关[15]。
其他的治疗建议包括:改变生活方式:常规运动、戒烟、限酒;每天补充600~1200mg的钙剂;每天补充400~800IU的Vit D,维持目标Vit D水平大于50~75nmol/L。评估措施包括:进行骨密度基线水平测定以及每1~2年一次的随访;当十年股骨头骨折概率大于等于3%或者骨质疏松相关骨折风险大于20%时考虑积极治疗干预。
三、心血管疾病
几乎所有的回顾性研究都提示ADT与心血管疾病相关。Keating等学者发表的大型观察性研究显示ADT将会增加心肌梗死的风险(风险比=1.09),患者死于心血管疾病的相对风险也将会增加。另一项近期的加拿大综述认为ADT将会增加31%的心梗风险以及16%的脑血管疾病风险[16]。当然也有相左的结论:随机对照试验的事后分析并未证实ADT与心血管事件的显著关联性[17]。
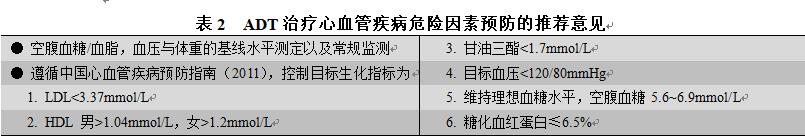
这种矛盾性的结果可能是因为ADT主要用于了不适合根治性治疗的(往往具有基础疾病)患者群体之中,而随机对照试验中的患者群体往往身体状态较好。值得指出的是,心血管疾病依然是前列腺癌患者最常见的非肿瘤死因。正如Nguyen指出的,接受ADT的人群中很有可能存在一部分心血管疾病易感亚组,需要针对这组患者密切监测发病风险[18]。2010年美国心脏协会发表在Circulation杂志上的论文也提及:ADT与心血管疾病以及相关死亡存在合理的关联性[17]。预防心血管副作用的推荐意见总结于表1。

(一)心血管疾病的危险因素:代谢综合征,糖尿病与肌萎缩性肥胖
1.代谢综合征代谢综合征在老年男性中较普遍,甚至在开始ADT前就存在[19]。代谢综合征的定义包括一系列生化指标变化与临床表现,比如血脂异常、高血压与糖尿病。ADT治疗后的患者容易出现HDL升高以及皮下脂肪的增加,这种表现与标准的代谢综合征不太一样,但是基于已知的代谢综合征与心血管疾病的关联来看,谨慎的处理与紧密的随访是合理的[20]。
2.高胆固醇血症空腹胆固醇的升高是是心血管事件死亡的独立危险因素,在中年以及老年人中更是如此。基线测定后,给予6个月的ADT可以使总胆固醇增加10.6%、甘油三酯增加26.9%、LDL增加7.3%、HDL增加10% [21]。虽然HDL的增加可能对于心脏有保护作用,但是总胆固醇、甘油三酯以及LDL的增加最终还是会损害患者的健康。
3.肥胖肌肉萎缩性肥胖是指肌肉组织减少而脂肪组织增加。大约70%的ADT患者会受此影响,身体肌肉脂肪构成比例发生巨大改变[22,23]。研究显示,ADT后肌肉组织减少2.7%而总体脂增加9.4%,总体重则增加2.4%。总体脂的增加可以归因于皮下脂肪的增加,特别时腰部的皮下脂肪的增加。肌肉萎缩可以导致肌力下降,无力,生存质量下降以及潜在的摔倒可能性的增加[23]。
4.糖尿病大型的队列研究显示,ADT与糖尿病发病存在显著相关性(风险比=1.44)[24]。前瞻性研究的结果也支持这样的结论,ADT可以增加空腹胰岛素的水平从而导致胰岛素抵抗的出现。在那些已有糖尿病的患者中,ADT会导致糖化血红蛋白的增加,血糖控制恶化以及糖尿病药物应用的增加[25]。相关推荐意见总结于表2。
(二)急性肾损伤
近期,Gandaglia与Lapi等学者强调了ADT可能诱发急性肾损伤[26,27]。当然肾功能损伤可能是由于尿路梗阻引起,而并非同时进行的ADT。而且晚期前列腺癌患者需要接受唑来膦酸治疗,这也是已知的可以导致急性肾损伤的药物。虽然该发现仍有争议,定期监测血清肌酐、尿蛋白水平和肾脏影像学检查还是必要的。慢性肾功能损伤与心血管疾病相关,也会增加ADT与心血管疾病死亡率的相关性。
四、新型内分泌治疗药物的副作用
阿比特龙是CYP17酶的特异性抑制剂,能够抑制多器官、多步骤的雄激素合成。在临床试验中,阿比特龙联合泼尼松治疗被报道具有乏力(39%)、关节痛(32%)、背痛(28%)、外周水肿(28%)、胃肠道不适(22%)、脸色潮红(22%)以及高血压(22%)等副作用[28]。总的来说,20%的患者报道了心脏功能的异常,比如心律失常、缺血性心脏病与心衰。而且,为了抵消可能的盐皮质过剩,需要每天同时服用10mg的泼尼松。长期的高剂量泼尼松可能会诱发骨质疏松、肥胖以及糖尿病等内分泌异常。
恩杂鲁胺是更为强力的雄激素受体拮抗剂,可以显著提升去势抵抗性前列腺癌患者的生存期。在最新的研究中,它的副反应包括乳房发育(36%)、乏力(34%)、乳头痛(19%)、潮热(18%)以及癫痫(1%)[29]。
结论
ADT在前列腺癌的综合治疗中起到了至关重要的作用。我国前列腺癌患者分期偏晚,中位年龄在70岁以上,常常合并多种系统疾病,早期识别和管理ADT的副作用变得比以往更加重要。同时,随着新型内分泌治疗药物更加普遍以及患者的生存期延长,ADT的时间也将会延长。在这种趋势下,关注到ADT的另一面,深入了解并进一步开展热点研究将是今后的重点。
参考文献
1. Llorente MD,Burke M,Gregory GR et al. Prostate cancer:a significant risk factor for late-life suicide. Am J Geriatr Psychiatry 2005;13:195-201.
2. Green HJ,Pakenham KI,Headley BC et al. Altered cognitive function in men treated for prostate cancer with luteinizing hormone-releasing hormone analogues and cyproterone acetate:a randomized controlled trial. BJU Int 2002;90:427-432.
3. Green HJ,Pakenham KI,Headley BC et al. Quality of life compared during pharmacological treatments and clinical monitoring for non-localized prostate cancer:a randomized controlled trial. BJU Int 2004;93:975-979.
4. Walker LM,Tran S,Robinson JW. Luteinizing hormone—releasing hormone agonists:a quick reference for prevalence rates of potential adverse effects. ClinGenitourin Cancer 2013;11:375-384.
5. Viani GA,Bernardes da Silva LG,Stefano EJ. Prevention of gynecomastia and breast pain caused by androgen deprivation therapy in prostate cancer:tamoxifen or radiotherapy? Int J RadiatOncolBiolPhys 2012;83:e519-524.
6. Irani J,Salomon L,Oba R et al. Efficacy of venlafaxine,medroxyprogesterone acetate,and cyproterone acetate for the treatment of vasomotor hot flushes in men taking gonadotropin-releasing hormone analogues for prostate cancer:a double-blind,randomised trial. Lancet Oncol 2010;11:147-154.
7. Cormie P,Galvao DA,Spry N et al. Can supervised exercise prevent treatment toxicity in patients with prostate cancer initiating androgen-deprivation therapy:arandomised controlled trial. BJU Int 2015;115:256-266.
8. Galvao DA,Spry N,Denham J et al. A multicentre year-long randomised controlled trial of exercise training targeting physical functioning in men with prostate cancer previously treated with androgen suppression and radiation from TROG 03.04 RADAR. EurUrol 2014;65:856-864.
9. Gardner JR,Livingston PM,Fraser SF. Effects of exercise on treatment-related adverse effects for patients with prostate cancer receiving androgen-deprivation therapy:a systematic review. J ClinOncol 2014;32:335-346.
10. Wadhwa VK,Weston R,Mistry R,Parr NJ. Long-term changes in bone mineral density and predicted fracture risk in patients receiving androgen-deprivation therapy for prostate cancer,with stratification of treatment based on presenting values. BJU Int 2009;104:800-805.
11. Hamilton EJ,Ghasem-Zadeh A,Gianatti E et al. Structural decay of bone microarchitecture in men with prostate cancer treated with androgen deprivation therapy. J ClinEndocrinolMetab 2010;95:E456-463.
12. Morote J,Morin JP,Orsola A et al. Prevalence of osteoporosis during long-term androgen deprivation therapy in patients with prostate cancer. Urology 2007;69:500-504.
13. Smith MR,Eastham J,Gleason DM et al. Randomized controlled trial of zoledronic acid to prevent bone loss in men receiving androgen deprivation therapy for nonmetastatic prostate cancer. J Urol 2003;169:2008-2012.
14. Smith MR,Egerdie B,Hernandez Toriz N et al. Denosumab in men receiving androgen-deprivation therapy for prostate cancer. N Engl J Med 2009;361:745-755.
15. Smith MR,Saad F,Oudard S et al. Denosumab and bone metastasis-free survival in men with nonmetastatic castration-resistant prostate cancer:exploratory analyses by baseline prostate-specific antigen doubling time. J ClinOncol 2013;31:3800-3806.
16. Jespersen CG,Norgaard M,Borre M. Androgen-deprivation therapy in treatment of prostate cancer and risk of myocardial infarction and stroke:a nationwide Danish population-based cohort study. EurUrol 2014;65:704-709.
17. Levine GN,D’Amico AV,Berger P et al. Androgen-deprivation therapy in prostate cancer and cardiovascular risk:a science advisory from the American Heart Association,American Cancer Society,and American Urological Association:endorsed by the American Society for Radiation Oncology. Circulation 2010;121:833-840.
18. Nguyen PL. Androgen-deprivation therapy and cardiovascular harm:let’s not throw out the baby with the bathwater. EurUrol 2014;65:710-712.
19. Cheung AS,Pattison D,Bretherton I et al. Cardiovascular risk and bone loss in men undergoing androgen deprivation therapy for non-metastatic prostate cancer:implementation of standardized management guidelines. Andrology 2013;1:583-589.
20. Tsai HT,Keating NL,Van Den Eeden SK et al. Risk of diabetes among patients receiving primary androgen deprivation therapy for clinically localized prostate cancer. J Urol 2015;193:1956-1962.
21. Smith MR,Finkelstein JS,McGovern FJ et al. Changes in body composition during androgen deprivation therapy for prostate cancer. J ClinEndocrinolMetab 2002;87:599-603.
22. Kim HS,Freedland SJ. Androgen deprivation therapy in prostate cancer:anticipated side-effects and their management. CurrOpin Support Palliat Care 2010;4:147-152.
23. Potosky AL,Knopf K,Clegg LX et al. Quality-of-life outcomes after primary androgen deprivation therapy:results from the Prostate Cancer Outcomes Study. J ClinOncol 2001;19:3750-3757.
24. Keating NL,O’Malley AJ,Smith MR. Diabetes and cardiovascular disease during androgen deprivation therapy for prostate cancer. J ClinOncol 2006;24:4448-4456.
25. Keating NL,Liu PH,O’Malley AJ et al. Androgen-deprivation therapy and diabetes control among diabetic men with prostate cancer. EurUrol 2014;65:816-824.
26. Gandaglia G,Sun M,Hu JC et al. Gonadotropin-releasing hormone agonists and acute kidney injury in patients with prostate cancer. EurUrol 2014;66:1125-1132.
27. Lapi F,Azoulay L,Niazi MT et al. Androgen deprivation therapy and risk of acute kidney injury in patients with prostate cancer. JAMA 2013;310:289-296.
28. Rathkopf DE,Smith MR,de Bono JS et al. Updated interim efficacy analysis and long-term safety of abiraterone acetate in metastatic castration-resistant prostate cancer patients without prior chemotherapy (COU-AA-302). EurUrol 2014;66:815-825.
29. Tombal B,Borre M,Rathenborg P et al. Enzalutamidemonotherapy in hormone-naive prostate cancer:primary analysis of an open-label,single-arm,phase 2 study. Lancet Oncol 2014;15:592-600.

叶定伟,教授,主任医师,博士生导师,复旦大学附属肿瘤医院副院长,泌尿外科主任,泌尿男生殖系统肿瘤多学科协作诊治中心首席专家,复旦大学前列腺肿瘤诊治研究中心主任,上海市抗癌协会前列腺肿瘤诊治中心主任,复旦大学泌尿外科研究所副所长,上海市抗癌协会理事长。上海市泌尿外科学会副主任委员,中国抗癌协会泌尿男生殖系肿瘤专业委员会候任主任委员,中国临床肿瘤学会肾癌专家委员会副主任委员,中国临床肿瘤学会(CSCO)免疫治疗专家委员会副主任委员,中国抗癌协会肿瘤分期专业委员会秘书长,中华医学会泌尿外科学会肿瘤专业委员会委员,中国老年肿瘤专业委员会常委,中国抗癌协会临床肿瘤协作专业委员会常委,泌尿疾病国际咨询委员会(ICUD) 委员,国际泌尿外科学会(SIU)协作咨询委员会委员,国家自然科学基金终审专家,中华医学科技奖评委,NCCN肾癌诊治指南中国版编写组副组长,NCCN前列腺癌及膀胱癌亚太诊治共识委员会委员,世界内镜医师协会中国协会泌尿科内镜与微创专业委员会理事,亚太前列腺癌学会(APPS)执行委员,亚洲冷冻治疗协会副主席,上海市领军人才,上海市医学领军人才,上海市优秀学科带头人。担任European Urology、Journal of Cellular and Molecular Medicine、Cancer Investigation、British Journal of Dermatology等著名SCI科学杂志的特约审稿人,《中华泌尿外科杂志》《中国癌症杂志》《临床肿瘤学杂志》《中华肿瘤防治杂志》《中华内镜杂志》《中华腔镜泌尿外科杂志》等多个权威杂志任编委。
来源:人民卫生出版社《临床知识》约稿
作者:叶定伟,复旦大学附属肿瘤医院副院长;朱耀;傅航成
编辑:环球医学资讯贾朝娟
- 评价此内容




 3我要打分
3我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号

 会员登录
会员登录

