【遏制细菌耐药白皮书】冯四洲教授:中性粒细胞缺乏患者抗菌药物合理应用
中性粒细胞缺乏是指外周血中性粒细胞绝对计数(Absolute Neutrophil Count,ANC)<0.5×109/L,或预计48小时后ANC<0.5×109/L;严重粒细胞缺乏指ANC<0.1×109/L。近年来,随着恶性血液病患者大剂量化疗及造血干细胞移植(Hematopoietic Stem Cell Transplant,HSCT),尤其半相合HSCT在国内的广泛开展,中心静脉导管与肠外营养临床应用的全面普及,中性粒细胞缺乏患者细菌、真菌、病毒、结核及结核分枝杆菌、原虫等病原微生物感染发生率呈现逐年增加的趋势。耐药细菌感染发生也呈增加的趋势,特别是耐碳氢霉烯肠杆菌科细菌(Carbapenem-Resistant Enterobacteriaceae,CRE)、多药耐药铜绿假单胞菌(Multi-Drug Resistant Pseudomonas Aeruginosa,MDR-PA)发生率明显增高,其菌血症及肺炎患者死亡率在30%~50%以上,严重威胁血液病患者生存,这些患者发生脓毒血症、感染性休克、重症肺炎是粒细胞缺乏感染患者中的危重症,尤其是严重粒缺且持续长时间者治疗尤为困难,死亡率更高。
一、中性粒细胞缺乏患者感染特点
血液病患者因疾病本身及相关治疗(大剂量化/放疗、中心静脉置管等)原因出现ANC缺乏或严重缺乏,皮肤黏膜屏障破坏,进食困难所致营养状态不佳,易发生感染而出现中性粒细胞缺乏发热(Febrile Neutropenia,FN)。中国血液病患者FN多中心前瞻性研究显示发热是血液病患者粒缺期常见的合并症,其中中心静脉置管、胃肠道粘膜炎、暴露于广谱抗菌素、粒缺持续时间>7天是血液病患者FN发生的独立危险因素,无任何危险因素、具备1项、2项、3~4项患者累计发热率依次增加(35.4%、69.2%、86.1%及95.6%,p<0.01),其中不明原因发热者占近三分之一(32.3%),最常见的感染部位依次是肺(49.5%)、上呼吸道(16%)、肛周组织(9.8%)、血流感染( Bloodstream Infection,BSI 7.7%)。最常见的病原微生物以革兰氏阴性菌为主,其次革兰氏阳性菌。此外,不同的感染部位病原菌的分布也明显不同:BSI主要以大肠埃希菌、肺炎克雷伯菌、表皮葡萄球菌、铜绿假单胞菌和白色念珠菌为主,而肺部感染主要以嗜麦芽窄食单胞菌、铜绿假单胞菌、鲍曼不动杆菌等非发酵菌为主。多因素分析显示年龄>40岁、血流动力学不稳定、既往耐药菌定植或感染、血流感染和肺炎是患者死亡独立危险因素。近年来耐药菌感染导致患者死亡率增加引起学者们广泛关注,CRE发病率及定植率均较高,2021CHINT数据显示肺炎克雷伯菌对亚胺培南与美罗培南耐药率分别达23.1%与24.4%;肠杆菌属细菌则分别达9.4%与9.6%;铜绿假单胞菌则分别达23%与18.9%,尤其是鲍曼不动杆菌则分别高达71.5%与72.3%。
二、FN患者感染抗菌药物应用前的评估
对于血液病FN患者在选择经验性抗菌药物治疗之前,许多问题必须考虑:FN感染的诊断及鉴别诊断;危险分层(低危或高危);详细询问病史并进行体格检查寻找可疑感染病灶;完成双套血细菌及真菌培养(建议连续两日进行,见附图1),血清GM、G试验、高分辨率CT等实验室检查;进行耐药评估(详见中国中性粒细胞缺乏伴发热抗菌药物临床应用指南2020版)及癌症患者支持治疗的多国协作组织(MASCC)危险指数评分(积分见附表1)。用药之前医生要充分考虑本病区及本医院的病原菌感染的流行病学特点、患者先前耐药病原菌尤其是多药耐药病原菌(Multidrug-resistant organisms,MDROs)感染与定植、先前抗菌药物使用情况及出现过敏与毒性发生情况。此外,医生选择何种药物对患者进行初始经验性治疗还要充分考虑患者的重要脏器功能状态、拟选择治疗药物在人体内PK/PD特点及药物相互作用、是否会对患者已经存在的脏器功能异常造成加重损害、拟选择的抗菌药物在可疑感染部位能否达到恰当的药物浓度等。
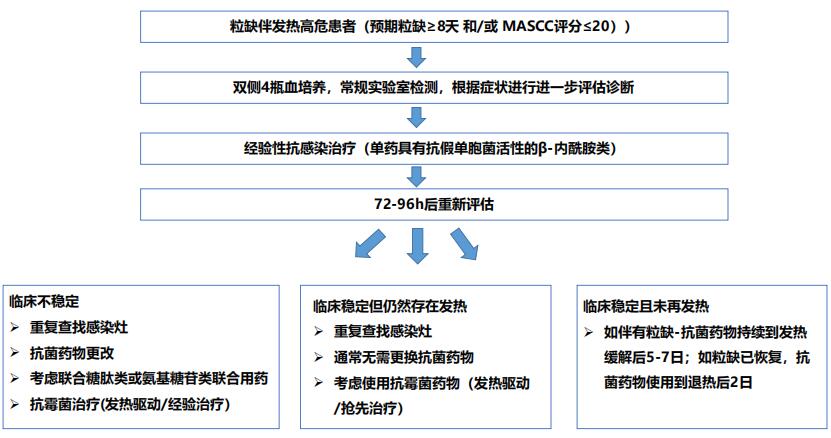
图1 粒缺发热患者初始经验性治疗后抗菌药调整及相关检查
表1 根据MASCC评分对粒缺伴发热患者进行风险分层

三、初始经验性抗菌治疗选择
1.高危患者(MASCC评分<21分)
(1)不明原因发热:高危患者必须立即住院治疗,各种评估完成后抗菌药物宜在FN发生后1小时内尽快应用,而不必等待微生物学检查的结果。对于不明原因的粒缺伴发热患者推荐单药治疗,起始给予具有抗假单胞菌活性的β-内酰胺制剂单药治疗或根据临床表现及MDROs感染的危险程度联合其他药物。对于无复杂感染的临床表现、无耐药菌感染的高危因素(存在耐药菌定植、有耐药菌感染病史)、本中心耐药菌感染率低且非重症患者,通常选择升阶梯抗感染治疗,建议经验性使用β-内酰胺酶抑制剂复合制剂(哌拉西林/他唑巴坦、头孢哌酮/舒巴坦)或抗假单胞菌头孢菌素如头孢吡肟、头孢他啶等广谱抗菌药物以降低碳氢霉烯类抗菌药物过度使用造成的细菌耐药率;对于临床表现为复杂感染、存在耐药菌定植、有耐药菌感染病史、耐药菌感染是本病区粒缺伴发热的常见原因的患者或尤其是患者临床表现较重的患者宜采取降阶梯策略,以改善预后,这些患者选择β-内酰胺类中的碳青霉烯类(亚胺培南-西司他丁、美罗培南),抗假单胞菌β-内酰胺类药物联合氨基糖苷类或喹诺酮类则是有效的替代。值得注意的是厄他培南不具备抗假单胞菌活性,应注意避免用于FN 患者经验性抗菌治疗。此外, FN患者也不宜采用氟喹诺酮类及氨基糖类药物单药经验性治疗。
FN患者初始经验性抗细菌治疗一般不推荐使用万古霉素等抗G+球菌药物。这是因为FN患者发生革兰阳性菌血症最常见致病菌为凝固酶阴性葡萄球菌,其相对毒力较弱,延迟治疗几日不会引起患者病情立即恶化,故无需立即使用万古霉素治疗;也有研究显示,初始经验性治疗给予抗假单胞菌活性β-内酰胺类药物,在加用或不加用万古霉素时,患者发热持续时间和死亡率无明显差异。但值得注意的是金黄色葡萄球菌引起的败血症休克等严重感染死亡率明显高于凝固酶阴性葡萄球菌,且具有耐甲氧西林金黄色葡萄球菌(Methicillin resistant Staphylococcus aureus,MRSA)定植的FN患者,经验性使用万古霉素等抗G+菌的药物患者则明显受益;采用喹诺酮类预防的患者易发生严重胃肠道粘膜炎,是发生草绿色链球菌菌血症的重要危险因素,且10%~25%的草绿色链球菌对青霉素及β-内酰胺类抗菌药物耐药,对氟喹诺酮类敏感性也较低,早期使用万古霉素等抗G+菌的药物治疗可使这类患者死亡率降低。因此,除上述两种情况外,在以下特定情况下FN患者初始经验性抗细菌治疗中应该使用万古霉素、替考拉宁、利奈唑胺或康替唑胺治疗。如血液动力学不稳定或严重脓毒血症、血培养证明存在革兰氏阳性菌感染,而最终鉴定结果和药敏结果尚未得到、怀疑严重导管相关血流感染、任何部位皮肤或软组织感染、眶周蜂窝组织炎等。值得注意的是万古霉素仍然是(Infectious Diseases Society of America,IDSA)推荐FN耐药G+菌感染治疗的重要药物,替考拉宁可作为万古霉素有效的替代治疗;利奈唑胺对MRSA肺炎患者疗效较万古霉素疗效更佳,肾毒性明显较低;达托霉素治疗MRSA血流感染、导管相关血流感染及皮肤软组织感染疗效明显优于万古霉素;康替唑胺对耐药G+菌肺炎及菌血症具有较好的疗效,且对造血干细胞移植早期患者的骨髓抑制作用较小,值得研究与应用。
(2)临床诊断感染:临床医生若发现患者存在可疑感染灶,经验性抗感染药物的选择参见附表2。
表2.根据感染灶进行经验性抗感染治疗推荐药物选择


(3)耐药菌定植或既往耐药菌感染:BSI患者FN初始经验性治疗选择药物不恰当是患者死亡的主要原因。国内有学者研究发现FN起始接受恰当(即敏感)抗菌药物治疗的患者,7 d死亡率仅为7.7%,明显低于72 h后才获得恰当抗菌药物治疗患者的29.9%(P<0.05) 。也有学者发现血液病伴耐碳青霉烯肺炎克雷伯菌(Carbapenem- Resistant Klebsiella Pneumonia,CRKP) BSI患者72 h后才得到恰当抗菌药物治疗的死亡率高达66.7%,明显高于24h内得到恰当抗菌药物治疗患者的29.1%(P<0.001) 。众多的研究均表明,起始不恰当使用抗菌药物的主要原因是耐药菌感染,特别是MDROs菌感染。意大利大系列HSCT患者的前瞻性研究表明,移植前具有CRKP定植者移植后粒缺期CRKP菌血症发生率明显高于与未定植者(32.5% vs. 0.1%,P<0.001)。异基因HSCT前具有耐碳青霉烯类铜绿假单胞菌(Carbapene Resistant Pseudomonas Aeruginosa,CRPA)定植者移植后粒缺期CRPA菌血症发生率明显高于无定植者(28.6% vs. 0.6%,P<0.001)。因此,关注患者既往耐药菌感染病史及此次粒缺发热前定植的MDROs菌对于选择合适的抗菌药物有重要作用。对于存在产超广谱β-内酰胺酶肠杆菌(Extended-Spectrum β-lactamase,ESBL-E)感染史或定植的患者初始经验性治疗选用哌拉西林-他唑巴坦治疗尤其延长滴注时间治疗可以获得与碳青霉烯类同等疗效,但目前多个重要国际指南仍推荐此类患者采用碳青霉烯类抗菌药物治疗,因此,哌拉西林-他唑巴坦至少可以作为脓毒血症或感染性休克患者等重症患者以外其他ESBL-E菌血症患者碳青霉烯类有效的替代手段,强烈推荐在合适的剂量条件下延长滴注时间;多部位CRE定植的高危重症患者建议采用至少两个CRE敏感药物(如氨基糖苷类、多黏菌素、替加环素、磷霉素或美罗培南等)联合治疗,或采用头孢他定-阿维巴坦单药2.5g q8h经验性治疗,值得一提的是头孢他啶-阿维巴坦只对产丝氨酸酶CRE有效,对于CRE产金属酶发生率较高的地区则需要采用头孢他啶-阿维巴坦联合氨曲南治疗,头孢他啶-阿维巴坦治疗CRE菌血症疗效优于其他药物的联合治疗,多黏菌素、替加环素这两药治疗CRE菌血症均不得单药治疗;高度怀疑存在其它耐药菌感染时采用如下方式选择抗菌药物:
①多重耐药铜绿假单胞菌(Multidrug Resistance Pseudomonas Aeruginosa,MDR-PA )(哌拉西林-他唑巴坦、头孢哌酮-舒巴坦、碳青霉烯类、头孢吡肟、头孢他啶等)之一联合氨基糖苷类或多黏菌素或磷霉素或采用新药头孢他定-阿维巴坦单药2.5g q8h治疗,头孢洛扎-他唑巴坦对MDR-PA具有较强抗菌活性,值得期待;全耐药铜绿假单胞菌(Pandrug resistant PA,PDR-PA)及泛耐药铜绿假单胞菌(extensively drug resistant PA,XDR-PA)治疗药物选择参见(中国中性粒细胞缺乏伴发热抗菌药物临床应用指南2020版)。
②多重耐药鲍曼不动杆菌(Multidrug Resistance Acinetobacter baumannii,MDR-AB) 美罗培南+多黏菌素、头孢哌酮-舒巴坦+多黏菌素、替加环素+多黏菌素等药物治疗;全耐药鲍曼不动杆菌(Pandrug resistant AB,PDR-AB)及泛耐药鲍曼不动杆菌(extensively drug resistant AB,XDR-AB)治疗药物选择参见(中国中性粒细胞缺乏伴发热抗菌药物临床应用指南2020版)。
③嗜麦芽窄食单胞菌 复方磺胺甲噁唑联合替卡西林/克拉维酸、头孢他啶或替加环素。MDR菌多部位定植而存在严重粘膜炎且怀疑BSI的患者应该根据定植耐药菌的药物敏感试验结果选择合适的抗菌药物联合治疗;出现感染性休克,如果存在耐药革兰氏阴性菌定植,通常可以根据定植菌的药敏选择两种敏感的药物联合治疗,尤其是有MDR定植菌的患者根据定植菌选择联合药物,必要时还可联合万古霉素等抗阳性菌药物及未采取抗真菌预防的患者加用棘白菌素类抗真菌药。
2.低危患者
根据MASCC积分指数≥21分或严重ANC缺乏≤7天者为低危组患者,给予口服抗菌药物门诊治疗48-72小时,通常给予具有抗假单胞菌活性的氟喹诺酮联合革兰阳性球菌药物(如氨苄西林/克拉维酸或克林霉素),而头孢呋辛或头孢克肟联合环丙沙星则作为替代治疗选择。如患者病情加重尽快住院治疗。
四、抗菌药物的调整
根据图1调整抗菌药物。病原菌已明确的FN患者抗菌药物选择参考中国中性粒细胞缺乏伴发热抗菌药物临床应用指南2020版。采用降阶梯策略治疗的患者如果病原菌明确则根据结果调整为窄谱抗菌药物,特别是重症感染多药联合治疗者,与此次感染治疗无关抗菌药物尽快停用。
五、抗菌药物预防与疗程
由于喹诺酮类抗菌药物对革兰阴性菌及革兰阳性菌耐药率均较高,不推荐粒缺患者广泛预防,尤其是低危粒缺患者不推荐抗菌药物预防。长期严重粒缺患者需充分考虑本地区氟喹诺酮类药物的敏感性,且明确抗菌药物预防仅降低FN菌血症的发生,并不降低死亡率,根据这些特点作出个体化抉择。值得一提的是采用氟喹诺酮类预防的中心必须进行流行病学监测,密切观察MDROs发生率的可能增加。
以往指南及学者们通常认为FN应该抗感染治疗至ANC恢复,但缺乏有力的证据支持。现在众多学者认为ANC恢复不是决定抗菌药物应用时间长短的先决条件。①不明原因FN患者,感染症状与体征消失,血流动力学稳定,退热5-7天后推荐停用抗菌药物;②不明原因FN患者,感染症状与体征消失,血流动力学稳定,退热72小时后也可以尝试停用抗菌药物;③临床证实的感染:感染的临床症状与体征消失后患者至少持续72小时以上无发热可以停用抗菌药物;④微生物证实的感染:感染的症状与体征消失,微生物清除,退热至少4天,抗菌药物治疗至少已7天可以停药;上述②③④这几种情况如果停药后粒缺持续,需密切观察患者24-48小时,如果再发FN,立即启动抗感染治疗。
此外值得注意的是抗菌药物的合理应用不能代替病灶的引流及必要的导管拔除。
参考文献:
1. 中华医学会血液学分会、中国医师协会血液科医师分会.中国中性粒细胞缺乏伴发热患者抗菌药物临床应用指南(2020年版). 中华血液学杂志2020; 41( 12): 969-977.
2. 冯四洲,陈欣. 血液病患者多药耐药革兰氏阴性菌感染经验性治疗策略.临床血液学杂志 2019;32(3):170-173.
3. 陈欣,冯四洲.中国中性粒细胞缺乏伴发热患者抗菌药物临床应用指南(2020年版)解读. 临床药物治疗杂志2021;19(9):14-17.
4. 王建祥主编. 血血系统疾病诊疗规范. 中国协和医科大学出版社 2020年11月第2版
5.Freifeld AG, Bow EJ, Sepkowitz KA, et al. Clinical Practice Guideline for the Use of Antimicrobial Agents in Neutropenic Patients with Cancer: 2010 Update by the Infectious Diseases Society of America. Clin Infect Dis 2011;52(4):e56–e93.
6. Escrihuela-Vidal F, Laporte J, Albasanz-Puig A, Gudiol C. Update on the management of febrile neutropenia in hematologic patients . Rev Esp Quimioter 2019;32 (Suppl. 2): 55-58.
7. Schmidt-Hieber M, Teschner D, Maschmeyer G & Schalk E. Management of febrile neutropenia in the perspective of antimicrobial de-escalation and discontinuation. Expert Rev Anti Infect Ther. 2019 ;17(12):983-995.
8. Martinez-Nadal G, Puerta-Alcalde P, Gudiol C, et al. Inappropriate Empirical Antibiotic Treatment in High-risk Neutropenic Patients With Bacteremia in the Era of Multidrug Resistance. Clinical Infectious Diseases 2020;70(6):1068–74.
9. Gudiol C, Aguilar-Guisado M, Azanza JR,et al. Executive summary of the consensus document of the Spanish Society of Infectious Diseases and Clinical Microbiology (SEIMC), the Spanish Network for Research in Infectious Diseases (REIPI) and the Spanish Society of Haematology and Haemotherapy (SEHH) on the management of febrile neutropenia in patients with hematological malignancies. Ennferm Infect Microbiol Clin 2020 ;38(4):174-181.
10. Peseski AM, McClean M, Green SD, et al. Management of fever and neutropenia in the adult patient with acute myeloid leukemia . Expert Rev Anti Infect Ther. 2021 ;19(3):359-378.
11. Hansen BA, Wendelbo Y, Bruserud Y, et al. Febrile Neutropenia in Acute Leukemia. Epidemiology, Etiology, Pathophysiology and Treatment. Mediterr J Hematol Infect Dis. 2020 ;12(1):e2020009.
12. Girmenia C, Bertaina A, Piciocchi A et al. Incidence, Risk Factors and Outcome of Pre-engraftment Gram-Negative Bacteremia After Allogeneic and Autologous Hematopoietic Stem Cell Transplantation: An Italian Prospective Multicenter Survey. Clin Infect Dis. 2017 ; 65(11):1884-1896.
13.Tang Y, Wu X, Cheng Q, et al. Inappropriate initial antimicrobial therapy for hematological malignancies patients with Gram-negative bloodstream infections. Infection 2020 ;48(1):109-116.
14.Falcone M, Bassetti M, Tiseo G, et al. Time to appropriate antibiotic therapy is a predictor of outcome in patients with bloodstream infection caused by KPC-producing Klebsiella pneumoniae. Crit Care. 2020 Jan 30;24(1):29.

北京协和医学院医学博士,二级主任医师,博士研究生导师
天津市首届名医,天津市第十七届人大代表
1999.7-2001.7在日本东京大学进行博士后研究
中国医学科学院血液病医院造血干细胞移植中心副主任
中国药理学会药源性疾病学专业委员会副主任委员
中国研究型医院学会血液病精准诊疗专业委员会副主任委员
中华医学会血液学分会抗感染学组副组长
中华医学会细菌感染与耐药防治分会委员
中国抗癌协会肿瘤血液病学专业委员会常委
中国老年医学学会血液病学分会移植感染专业委员会副主任委员
中国老年医学学会血液病学分会常委
中国临床肿瘤学会抗白血病联盟专家委员会常委
中国医药教育协会造血干细胞移植及细胞治疗专业委员会常委
海峡两岸医药卫生交流协会血液病学专业委员会常委
天津市抗癌协会老年肿瘤专业委员会主任委员
天津市中西医结合学会血液病专业委员会副主任委员
中华器官移植杂志、临床血液学杂志、生物医学工程与临床杂志、
内科急危重症杂志、淋巴瘤&白血病杂志编委
发表核心期刊论文及SCI论文150余篇,获省部级科技进步奖5项
来源:人民卫生出版社《临床知识》约稿
作者:冯四洲,中国医学科学院血液病医院;陈欣,徐春晖
编辑:环球医学资讯余霞霞
- 评价此内容




 3我要打分
3我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号

 会员登录
会员登录

