王长利教授:非小细胞肺癌新辅助免疫治疗进展与展望
肺癌是全世界范围内发病率和死亡率最高的恶性肿瘤,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)占80%~85%[1,2]。免疫治疗已经被证实在部分晚期NSCLC中显著延长患者无进展生存期(progression free survival,PFS)及总生存期(overall survival,OS)[3-7]。早期NSCLC患者的5年生存率随着临床分期的上升而下降,从IA期的80%~90%下降到ⅢA期的40%,并且30%~60%早期NSCLC患者术后仍面临肿瘤复发转移的问题[8]。传统的术前新辅助治疗虽然可以提高早期NSCLC患者5.4%的生存率,却不可避免的伴随着高于60%的Ⅲ级及更高级别治疗相关毒性的发生率[9,10]。因此如何优化早期NSCLC患者术前新辅助治疗策略就成为了亟需解决的问题。自2018年以来,免疫治疗开始在早期NSCLC新辅助治疗中崭露头角。现就NSCLC新辅助免疫治疗的研究进展及展望综述如下。
一、传统NSCLC新辅助治疗的获益与风险
1.传统NSCLC新辅助治疗的获益
为了最优化治疗效果,对于可切除NSCLC患者的新辅助治疗概念在2000年被重新提出,即NSCLC术前给予全身或局部治疗,用以区别于术后辅助治疗。理论上,NSCLC新辅助治疗可以使患者获益如下:①使肿瘤体积缩小,提高手术的可切除性;②消灭或预防微转移灶;③提高患者治疗耐受性;④术前因肿瘤血供保持完整,治疗药物更有效地到达病灶[11,12]。
2.传统NSCLC新辅助治疗的风险
传统NSCLC新辅助治疗存在以下风险:①新辅助治疗后导致肿瘤分期不准确;②手术延迟;③新辅助治疗后肿瘤可能无法切除;④治疗相关毒性增加[11,12]。尤其对于N2期的NSCLC新辅助治疗仍然没有定论。早期的Ⅱ期临床试验研究结果显示术前新辅助放化疗可以提高手术获益,但是随之扩大样本的Ⅲ期临床试验结果并没有观察到同样的临床获益[13-17]。
应用目前方案新辅助治疗策略ⅢA期NSCLC患者的5年生存率仅为36%左右[18]。然而新辅助免疫治疗有可能弥补这些传统新辅助治疗的不足,降低新辅助治疗毒性并提高手术切除概率,延长患者生存。
二、NSCLC新辅助免疫治疗的合理性
1.免疫检查点抑制剂PD-1/PD-L1抗体的免疫治疗在部分晚期NSCLC中诱导持续缓解为其在NSCLC的早期应用提供了可能性
Nivolumab,Atezolizumab以及Pembrolizumab(PD-L1≥1%)相比于多西他赛在晚期肺癌二线治疗中延长了总生存[19]。
Pembrolizumab相比于化疗在PD-L1≥50%的晚期NSCLC中总生存有绝对获益;数据报道在PD-L1≥1%的晚期NSCLC患者中Pembrolizumab也显示了生存的获益[20]。
非鳞非小细胞肺癌一线治疗:Pembrolizumab联合化疗相比化疗延长总生存[21];Atezolizumab联合化疗及贝伐单抗延长无进展生存[22]。
Nivolumab联合Ipilizumab相比化疗在TMB≥10/Mb的一线NSCLC中延长无进展生存[23]。
2.Ⅰ-Ⅲ期NSCLC患者新辅助免疫治疗的合理性
目前对于可切除肺癌的系统治疗没有治疗进展,但是大部分患者在局部治疗后出现复发转移。对于早期NSCLC患者可能拥有更完整的免疫系统。
对微小转移灶有更大的潜能诱导免疫激活。
新辅助治疗为开展相关科学研究创造了理想的机会。
临床前研究已经在小鼠乳腺癌模型中证实PD-1抗体联合CD137抗体的新辅助治疗比辅助治疗更能够有效的清除转移灶[24]。
3.新辅助免疫治疗已经在其他早期实体瘤中被证实临床获益
Ipilizumab新辅助治疗与安慰剂相比,可以使恶性黑色素瘤患者5年OS从54%延长至65%[25]。
906例术后的ⅢB-Ⅳ期恶性黑色素瘤患者被随机至Ipilimumab或者Nivolumab组,1年的无复发生存分别为60%和70%[26]。
早期恶性黑色素瘤患者,手术之后使用PD-1抗体治疗,死亡或者复发风险降低了43%[27]。
Pembrolizumab联合化疗在早期乳腺癌的新辅助治疗中可以使病理完全缓解率(pathologic complete response,pCR)提高2~3倍[28]。
三、NSCLC新辅助免疫治疗的研究终点
无病生存(disease free survival,DFS)和OS是早期肺癌临床试验的长期研究终点,但其经常需要经过数年才能获得成熟数据。
pCR等替代终点已成为乳腺癌新辅助治疗的研究终点。
pCR在肺癌中非常罕见,但约20%的化疗患者可以达到病理大缓解(major pathologic response,MPR,原发灶中≤10%活细胞)并且可以预测疾病无进展生存(disease free survival,DFS)[29]。
免疫相关病理缓解(Immune-Related Pathologic Response Criteria,irPRC)有可能取代OS成为新的新辅助免疫治疗研究终点[30]。
四、NSCLC新辅助免疫治疗的临床研究进展
《新英格兰医学杂志》近期发表了一项关于早期NSCLC新辅助免疫治疗的风暴式研究成果[31]。这个临床试验设计特别,在需要手术的患者术前应用PD-1抗体Nivolumab进行治疗,目的是追踪观察Nivolumab对这些病人新辅助免疫治疗的应答。该试验共招募21例Ⅰ期-ⅢA期的NSCLC患者,其中62%是腺癌,81%为ⅡA期-ⅢA期患者。手术前4周给予患者Nivolumab治疗,治疗剂量3mg/kg,每2周一次。研究者分别采集患者开始Nivolumab治疗前的穿刺活检病理标本及手术后标本进行详细的基因检测及免疫分析等,从而对比出用药前后患者的各种变化。21例患者中的20例患者按原计划进行了手术,其中一位患者由于出现了Ⅲ级免疫相关性肺炎,提前进行了手术。总的来说,术前使用Nivolumab并不影响正常的手术计划。治疗前后影像学评估显示:2例(10%)患者肿瘤部分缓解、18例(85%)患者肿瘤稳定、1例患者肿瘤进展。从影像学上判断,术前新辅助Nivolumab疾病控制率达到96%。而影像学上提示经过免疫治疗后疾病进展的患者,术后病理发现组织绝大部分都是免疫细胞,癌细胞已经基本坏死。在20例按照计划进行手术的患者中,研究者对比了用药前和手术后的病理切片,发现Nivolumab治疗之后,9/21例(43%,95%CI 24%~63%)患者MPR,2/20例患者复发。有3例患者肿瘤细胞全部坏死。进一步分析发现新辅助免疫治疗的临床疗效与肿瘤突变负荷呈正相关,即肿瘤突变负荷越高的患者临床获益越显著。在安全性方面,20例患者中只有1例患者出现了3级不良反应,没有4或5级毒性发生,Nivolumab应用于NSCLC新辅助免疫治疗的安全性非常好。基于这些令人欢欣鼓舞的数据,申办方已经扩大患者样本量并联合ipilizumab进一步观察临床研究结果。这项研究得到了世界癌症治疗顶级机构约翰霍普金斯大学和纪念斯隆凯特琳癌症中心的机构审查委员会的批准。
科学家们发现,接受Nivolumab治疗起效的患者其肿瘤组织及外周血中特异性杀伤肿瘤细胞的T细胞数量和比例相较于治疗无效的患者显著提高。尤其是那些能特异性针对所谓肿瘤新生抗原的T细胞的激活和扩增尤其明显。这说明Nivolumab新辅助治疗成功的关键在于T细胞在手术后通过外周血、循环到患者的整个身体,从而攻击肿瘤细胞并防止新的转移。研究者认为Nivolumab有效地将肺部肿瘤转化为“自动疫苗”,从而杀死体内的肿瘤细胞。在手术前通过免疫疗法激活的T细胞可以在患者手术后在整个机体内截留逃亡的肿瘤细胞,并防止癌症复发,这可能是一个改变游戏规则的治疗策略。
另一项有里程碑意义的新辅助免疫治疗研究成果见于Durvalumab的PACIFIC研究。PACIFIC研究[32]是一项随机、双盲、安慰剂对照的国际多中心临床研究,2∶1随机,评估Durvalumab作为维持治疗用于接受了标准的含铂方案同步放化疗后,未发生疾病进展的无法手术切除的局晚期(Ⅲ期)非小细胞肺癌者。该研究达到研究终点,与标准治疗相比,Durvalumab延长无疾病进展生存超过11个月(16.8个月vs 5.6个月;HR=0.62;95%CI 0.42~0.65)。Durvalumab对比安慰剂组,显著提高ORR,两组分别为28.4%和16%(RR=1.78;95%CI 1.27~2.51)。此外,评估两组至患者死亡或远处转移的时间,Durvalumab组亦显著优于安慰剂组(23.2个月vs 14.6个月;HR=0.52;95%CI 0.39~0.69,P<0.0001)。基于此Durvalumab目前已经被FDA批准用于不可切除的Ⅲ期NSCLC。
五、NSCLC新辅助免疫治疗的研究展望
除了我们详细介绍过的Nivolumab单药临床试验的中期数据,目前还有其他两个Nivolimab联合Ipilimumab的临床试验正在开展。CheckMate816是一个随机开放的Ⅲ期临床试验。试验组是Nivolimab联合Ipilimumab新辅助治疗,对照组是标准的含铂双药化疗。招募入组患者是ⅠB~ⅢA期NSCLC。CheckMate816试验设计是基于CheckMate012,一个ⅢB/Ⅳ期患者的Ⅰ期临床试验的数据显示双免疫联合治疗可以获得更高的客观缓解率及PFS[33]。此研究的首要研究终点是手术时的pCR。正在开展的另一项NEOSTAR试验(NCT03158129)则在Ⅰ-ⅢA期NSCLC患者中对比Nivolimab联合Ipilimumab与Nivolimab单药的新辅助治疗的临床疗效。
TOP1501(NCT02818920),一个Ⅱ期试验正在试图评价Pembrolizumab新辅助后手术的切除率及序贯Pembrolizumab辅助治疗的临床疗效。
Atezolizumab也在新辅助治疗阶段开展很多Ⅱ期临床试验。PRINCEPES试验(NCT02994576)给患者一个剂量的Atezolizumab新辅助治疗,而另一个试验(NCT02927301)则给患者两个剂量的Atezolizumab新辅助治疗,术后给予新辅助化疗并序贯Atezolizumab巩固维持到1年[34]。
Durvalumab目前成为第一个被美国FDA批准应用于不可切除的Ⅲ期NSCLC的免疫治疗药物。其另外的一个Ⅱ期的新辅助及辅助临床试验(NCT02572843)正在瑞士开展。该试验设计是针对ⅢA期患者Durvalumab联合化疗新辅助,术后再序贯Durvalumab辅助治疗。
表1列举出了全球正在进行的早期NSCLC新辅助免疫临床试验。
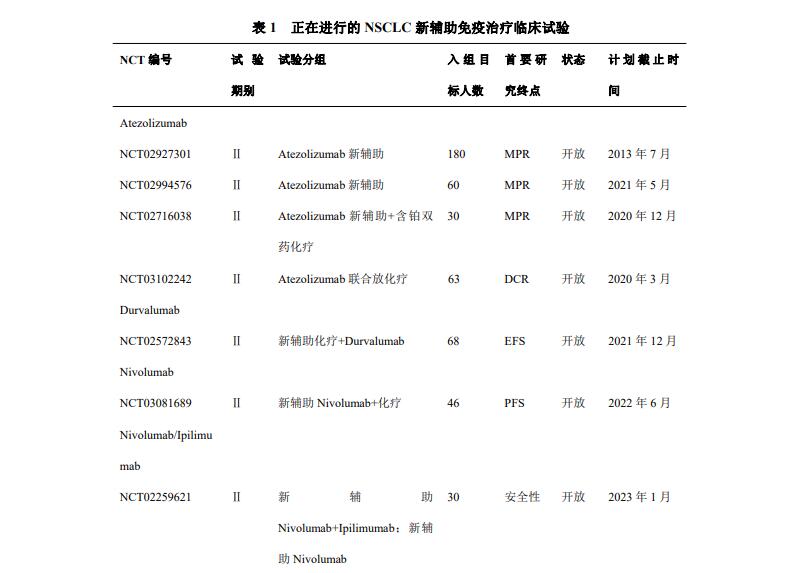
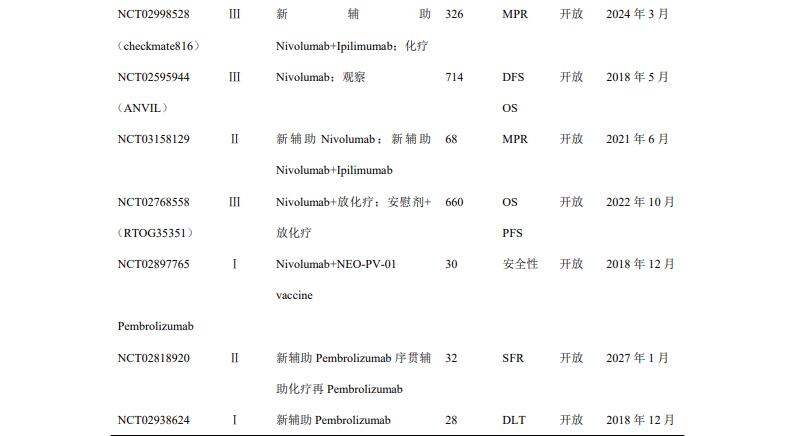
注:SFR:surgical feasibility rate,可手术切除率;DLT:dose limited toxicity,剂量限制性毒性
六、结论
大量免疫检查点抑制剂在NSCLC新辅助治疗阶段的临床试验正在如火如荼的开展。尽管目前数据仍然非常有限,但一些中期数据分析已经显示出了非常好的治疗效果及耐受良好的毒性,并且为手术切除提供了更好的空间。对于不可切除的Ⅲ期NSCLC患者,PACIFIC研究已经达到了其研究终点PFS,美国FDA也即将批准其临床应用于这一领域。除了Nivolumab,Atezolizumab,Pembrolizumab也已经在NSCLC新辅助治疗领域开展临床研究。在未来的3~6年里,数个临床研究结果即将揭晓谜底。随着这些大型临床数据结果的陆续公布,相信我们即将看到NSCLC新辅助免疫治疗的曙光。
参考文献
[1] Howlader N,NooneAM,Krapcho M,et al. SEER Cancer Statistics Review(CSR),1975-2014. Bethesda:National Cancer Institute,2017.
[2] Jemal A,Bray F,Center MM,et al. Global cancer statistics. CA Cancer J Clin,2011;61:69-90.
[3] Gettinger SN,Horn L,Gandhi L,et al. Overall survival and long-term safety of nivolumab(anti-programmed death 1 an-tibody,BMS-936558,ONO-4538) in patients with previously treated advanced non-small-cell lung cancer. J ClinOncol,2015,33:2004-2012.
[4] Rittmeyer A,Barlesi F,Waterkamp D,et al. Atezolizumab versus docetaxel in patients with previously treated non-small-cell lung cancer(OAK):a phase 3,open-label,multicentrerandomised con-trolled trial. Lancet,2017,389:255-265.
[5] Reck M,Rodríguez-Abreu D,Robin-son AG,et al. Pembrolizumab versus chemotherapy for PD-L1-positive non-small-cell lung cancer. N Engl J Med,2016,375:1823-1833.
[6] Antonia SJ,Villegas A,Daniel D,et al. Durvalumab after chemoradiotherapy in stage Ⅲ non-small-cell lung cancer. N Engl J Med,2017,377:1919-1929.
[7] Garon EB,Rizvi NA,Hui R,et al. Pembrolizumab for the treatment of non-small-cell lung cancer. N Engl J Med,2015,372:2018-2028.
[8] Goldstraw P,Crowley J,Chansky K,et al. The IASLC Lung Cancer Staging Project:proposals for the revision of the TNM stage groupings in the forthcoming(sev-enth) edition of the TNM Classification of Malignant Tumours. J ThoracOncol,2007,2:706-714.
[9] Pignon JP,Tribodet H,Scagliotti GV,et al. Lung adjuvant cisplatin evaluation:a pooled analysis by the LACE Collaborative Group. J ClinOncol,2008,26:3552-3559.
[10] Wakelee HA,Dahlberg SE,Keller SM,et al. Adjuvant chemotherapy with or without bevacizumab in patients with reected non-small-cell lung cancer(E1505):an open-label,multicentre,randomised,phase 3 trial. Lancet Oncol 2017,18:1610-1623.
[11] Mcelnay P,Lim E. Adjuvant or neoadjuvant chemotherapy for NSCLC J Thorac Dis,2014,6(suppl 2):S224-227.
[12] Salva F,Felip E. Neoadjuvant chemotherapy in early-stage non-small cell lung cancer.Transl Lung Cancer Res 2013,2(5):398-402.
[13] Albain KS,Swann RS,Rusch VW,et al. Radiotherapy plus chemotherapy with or without surgical resection for stage
Ⅲ non-small-cell lung cancer:a phase Ⅲrandomised controlled trial. Lancet 2009,374:379-386.
[14] Burkes RL,Shepherd FA,Blackstein ME,et al. Induction chemotherapy with mitomycin,vindesine,and cisplatin
for stageⅢA(T1-3,N2)unresectable non-small-cell lung
cancer:final results of the Toronto phaseⅡ trial. Lung 29. Cancer 2005,47:103-109.
[15] Eberhardt WE,Pottgen C,Gauler TC,et al. PhaseⅢ Study of Surgery Versus Definitive Concurrent Chemoradiotherapy Boost in Patients With Resectable 30. StageⅢA(N2) and Selected ⅢB Non-Small-Cell Lung
Cancer After Induction Chemo-therapy and Concurrent Chemoradiotherapy(ESPATUE). J ClinOncol,2015,33:4194-4201.
[16] vanMeerbeeck JP,Kramer GW,Van Schil PE,et
al. Randomized controlled trial of resection versus
radiotherapy after induction chemotherapy in stage 32. ⅢA-N2 non-small-cell lung cancer. J Natl Cancer Inst 2007,99:442-450. 33.
[17] Weder W,Collaud S,Eberhardt WE,et al.
Pneumonectomy is a valuable treatment option after
neoadjuvant therapy for stage Ⅲ non-small-cell lung
cancer. J ThoracCardiovascSurg 2010,139:1424-1430.
[18] Goldstraw P,Chansky K,Crowley J,et al. The IASLC Lung Cancer Staging Project:Proposals for Revision of the TNM Stage Groupings in the Forthcoming(Eighth) Edition of the TNM Classification for Lung Cancer. J ThoracOncol 2016,11:39-51.
[19] IPassiglia F,Galvano A,Rizzo S,et al. Looking for the best immune-checkpoint inhibitor in pre-treated NSCLC patients:An indirect comparison between nivolumab,pembrolizumab and atezolizumab. Int J Cancer,2018,142(6):1277-1284.
[20] Hui R,Garon EB,Goldman JW,et al. Pembrolizumab as first-line therapy for patients with PD-L1-positive advanced non-small cell lung cancer:a phase 1 trial. Ann Oncol,2017,28(4):874-881.
[21] Gandhi L,Rodríguez-Abreu D,Gadgeel S,et al. KEYNOTE-189 Investigators.Pembrolizumab plus Chemotherapy in Metastatic Non-Small-Cell Lung Cancer. N Engl J Med,2018,378(22):2078-2092.
[22] Liu SV,Camidge DR,Gettinger SN,et al. Long-term survival follow-up of atezolizumab in combination with platinum-based doublet chemotherapy in patients with advanced non-small-cell lung cancer.Eur J Cancer,2018,101:114-122.
[23] Hellmann MD,Ciuleanu TE,Pluzanski A,et al. Nivolumab plus Ipilimumab in Lung Cancer with a High Tumor Mutational Burden. N Engl J Med,2018,378(22):2093-2104.
[24] Liu J,Blake SJ,Yong MC et al. Improved Efficacy of Neoadjuvant Compared to Adjuvant Immunotherapy to Eradicate Metastatic Disease. Cancer Discov,2016,6(12):1382-1399.
[25] Retseck J,Nasr A,Lin Y,et al.Long term impact of CTLA4 blockade immunotherapy on regulatory and effector immune responses in patients with melanoma. J Transl Med,2018,16(1):184.
[26] Meerveld-Eggink A,Rozeman EA,Lalezari F et al. Short-term CTLA-4 blockade directly followed by PD-1 blockade in advanced melanoma patients:a single-center experience. Ann Oncol,2017,28(4):862-867.
[27] Eggermont AMM,Blank CU,Mandala M,et al.,Adjuvant Pembrolizumab versus Placebo in Resected Stage ⅢMelanoma. N Engl J Med,2018,378(19):1789-1801.
[28] Role for Immune Therapy in Advanced Breast Cancer. Cancer Discov,2018,8(2):132-133.
[29] Pataer A1,Kalhor N,Correa AM,et al. Histopathologic response criteria predict survival of patients with resected lung cancer after neoadjuvant chemotherapy. J ThoracOncol,2012,7(5):825-832.
[30] T.R. Cottrel,E.D. Thompson,P.M. Forde et al. Pathologic Features of Response to Neoadjuvant Anti-PD-1 in Resected Non-Small Cell Lung Carcinoma:A Proposal for Quantitative Immune-Related Pathologic Response Criteria(irPRC). Ann Oncol,2018.
[31] P.M. Forde,J.E. Chaft,K.N. Smith,et al. Neoadjuvant PD-1 Blockade in Resectable Lung Cancer. N Engl J Med,2018,378(21):1976-1986.
[32] Antonia SJ,Villegas A,Daniel D,et al. Durvalumab after Chemoradiotherapy in Stage Ⅲ Non-Small-Cell Lung Cancer. N Engl J Med,2017,377:1919-1929.
[33] Hellmann MD,Rizvi NA,Goldman JW,et al. Nivolumab plus ipilimumab as first-line treatment for advanced non-small-cell lung cancer(CheckMate 012):results of an open-label,phase 1,multicohort study. Lancet Oncol,2017,18:31-41.
[34] Owen DH,Bunn PA,Johnson BE,et al. A phase Ⅱ study of atezolizumab as neoadjuvant and adjuvant therapy in patients(pts) with resectable non-small cell lung cancer(NSCLC). Chicago:2017 ASCO Annual Meeting,2017.

王长利
教授、博士生导师,天津医科大学肿瘤医院肺部肿瘤科主任医师,国家级重点专科胸外科学科带头人。兼任中国抗癌协会肺癌专业委员会前任主任委员,CSCO非小细胞肺癌专业委员会副主任委员,天津市抗癌协会肺癌专业委员会主任委员,天津市肺癌诊疗中心主任,天津医学会胸外科学会副主任委员。
一直从事胸部肿瘤临床外科工作,主要从事肺癌早期诊断、外科治疗、综合治疗及肺癌相关基础研究与临床研究。参与制定《CSCO肺癌指南》《EGFR突变和ALK融合基因阳性非小细胞肺癌的诊断和治疗指南指南》《中国间变性淋巴瘤激酶(ALK)阳性非小细胞肺癌诊疗指南》等诊疗规范。在国内外重要期刊发表论文80余篇,主编《肺癌》,参编《肿瘤手术学》等专著。担任《中华外科杂志》《癌症》等编委会委员。承担了国家、市级和局级等各级科研课题多项。
来源:人民卫生出版社《临床知识》约稿
作者:王长利教授,天津医科大学肿瘤医院肺部肿瘤科主任医师;韩颖
编辑:环球医学资讯丁好奇
- 评价此内容




 3我要打分
3我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号

 会员登录
会员登录

