左腰背部酸胀感1年余 居然是肿瘤
老年女性,左腰背部酸胀感1年余,未行特殊处理,无腹痛等不适,无恶心呕吐,无畏寒、发热、盗汗,无咳嗽、咳痰。影像学发现胰腺尾部占位,如何进一步明确病变来源及性质?
患者,女,63岁,汉族人。主诉:左腰背部酸胀感1年余。
入院情况:患者于1年前无明显诱因感腰背部酸胀,未行特殊处理,无腹痛等不适,无恶心呕吐,无畏寒、发热、盗汗,无咳嗽、咳痰。近来自觉症状较前明显,于当地医院行上腹部CT示:胰尾部可见一类圆形囊实性低密度影,直径约3.8cm,增强后囊壁及实性部分可见强化。诊断:胰腺尾部囊实性占位。腹部MRI示:胰腺尾部区域见一类圆形囊实性信号影,大小约3.7cm×3.0cm,动脉期病灶实质部分不均匀明显强化,门脉期及延迟期呈持续性、渐进性强化,考虑:胰腺尾部区域占位,考虑来源于胰腺肿瘤,不除外腹腔间质瘤的可能。遂就诊于我院。患者既往健康状况良好,否认有特殊食物、药物过敏史。家族史及个人史:无特殊。入院查体: T 36.7℃,P 81次/分,R 19次/分,BP 130/ 86mmHg。一般状况良好,发育正常,全身皮肤未见明显黄染,未见皮疹及出血点,无肝掌、蜘蛛痣。巩膜未见明显黄染,心肺无异常。腹平坦,无腹壁静脉曲张,腹部柔软,无明显压痛、反跳痛,腹部无包块。肝脾肋下未触及,Murphy征阴性,肾区无叩击痛,移动性浊音阴性。肠鸣音未见异常,4次/分。入院后化验血常规:白细胞3.04×109/L,中性粒细胞50.0%;血小板170×109/L,血红蛋白118g/L。尿常规正常。便常规正常,潜血阴性,红细胞、白细胞阴性。肝肾功能:总胆红素10.8μmol/L,结合胆红素2.9μmol/L,白蛋白42g/L,丙氨酸转氨酶23U/L,天冬氨酸转氨酶35U/L,γ-谷氨酰转肽酶15U/L,碱性磷酸酶44U/L,肌酐50μmol/L,尿素5.5mmol/L。血糖类抗原CA19-9 21.53U/ml,癌胚抗原0.50μg/L。
初步诊断:本例患者无特异性症状,以肿瘤压迫症状为主,影像学发现胰腺尾部占位,目前诊断考虑:①胰尾囊实性占位;②腹腔及腹膜后占位;需进一步明确病变来源及性质。为了明确诊断,必要的检查包括血尿便常规、肝肾功能、肿瘤标志物;腹部B超或CT、MRI、上消化道内镜如EUS,必要时细针穿刺活检等。
鉴别诊断:该患者以影像学发现胰尾囊实性占位而就诊,首先应明确病变的来源及性质。病变可能为来源于胰腺的囊性肿瘤或实性肿瘤囊性变,或者为来源于腹腔及腹膜后的肿瘤性病变。胰腺囊性肿瘤是指一类胰管或腺泡组织上皮细胞增生致使分泌物潴留而发生的肿瘤性囊性病变,是一种少见的肿瘤。常见的胰腺囊性肿瘤为胰腺囊腺瘤和囊腺癌、胰腺实性假乳头肿瘤和胰腺导管内乳头状黏液性肿瘤。胰腺囊腺瘤和囊腺癌是一种少见的肿瘤,Compagno等于1978年结合临床预后将其分为胰腺浆液性囊腺瘤和胰腺黏液性囊腺瘤两类,后者又分黏液性囊腺瘤和黏液性囊腺癌。实性假乳头肿瘤(solid pseudopapillary tumor of pancreas,SPT)是一种实体肿瘤,多发于年轻女性,常见于胰头部,CT检查显示为胰腺囊实性肿瘤,边界清晰、包膜完整,肿瘤实性部分和包膜有钙化,增强后明显强化; MRI检查显示肿瘤内有分层现象,内镜超声除可了解肿瘤与胃、胰腺的关系和定位外,尚表现为不规则、厚壁的囊实性肿瘤,并可有高回声的钙化环,结合临床患者为年轻女性则要高度怀疑为SPT。胰腺导管内乳头状黏液性肿瘤(intraductal papillary mucinous neoplasms,IPMN)是近几年被认识的一种胰腺囊性肿瘤。根据肿瘤起源不同,通常将胰腺导管内乳头状黏液性肿瘤分为3种类型:主胰管型、分支胰管型、混合型。1996年日本胰腺学会从病理学上将产黏液胰腺肿瘤分为增生型、腺瘤型和腺癌型。同年,WHO从组织学上将其分为导管内乳头状黏液瘤、交界性和导管内乳头状黏液癌。一些来源于胰腺的实性肿瘤如胰腺癌甚至胰腺内分泌肿瘤有时均可因变性、坏死等在临床表现为囊性肿瘤。病理上也可因囊性变而与原形态有很大不同,故此类肿瘤亦应给予足够的重视。虽然患者目前所发现的占位位于胰尾可能性大,但也有可能为起源于腹腔的肿瘤如腹腔间质瘤;或起源于腹膜后的病变如神经鞘瘤、恶性转移癌、神经纤维肉瘤及横纹肌肉瘤等。
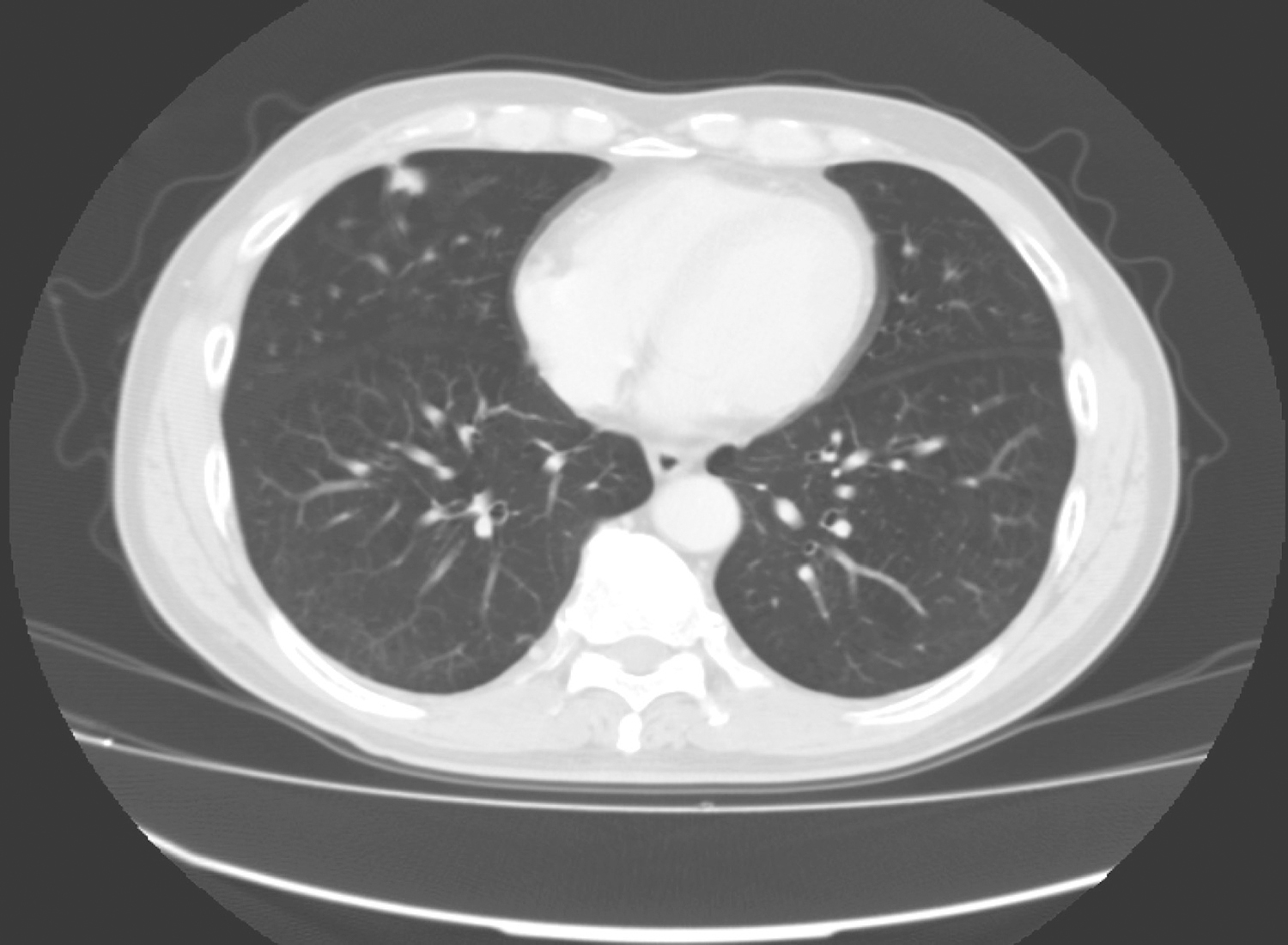
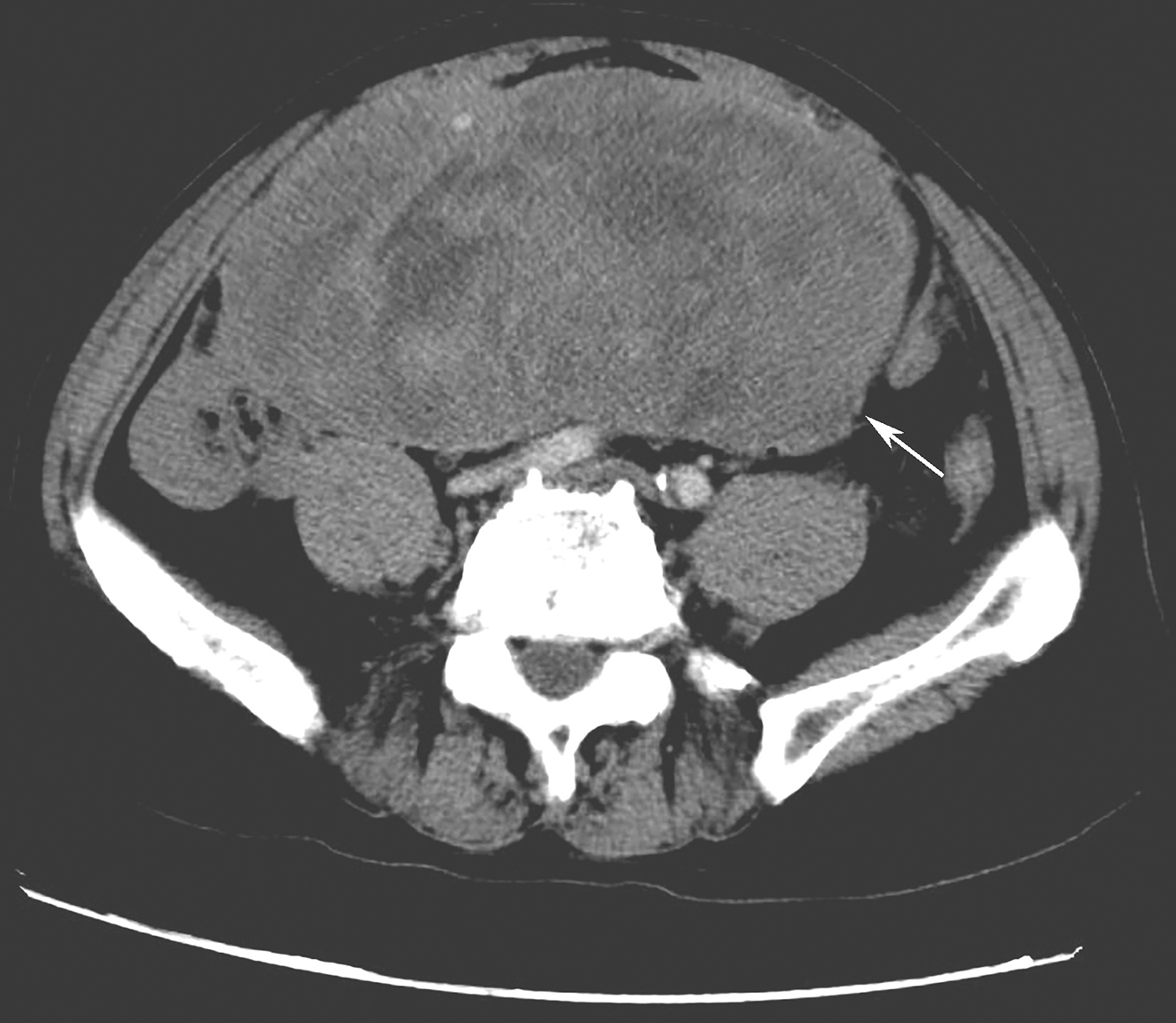
诊疗经过:辅助检查:心电图正常。胸片心肺膈未见异常。腹部B超提示:脾肾间隙囊实性占位,考虑来源于胰腺;肝胆脾肾未见异常。上腹部增强CT提示胰腺尾部见范围26mm×32mm混杂密度肿块,边界清晰,增强后明显不均匀强化,胰管轻度扩张。腹膜后未见增大淋巴结影。诊断为:胰尾部囊实性病灶,实性假乳头肿瘤可能(图3-32-1)。
图3-32-1 CT示:胰尾部囊实性病灶,实性假乳头肿瘤可能
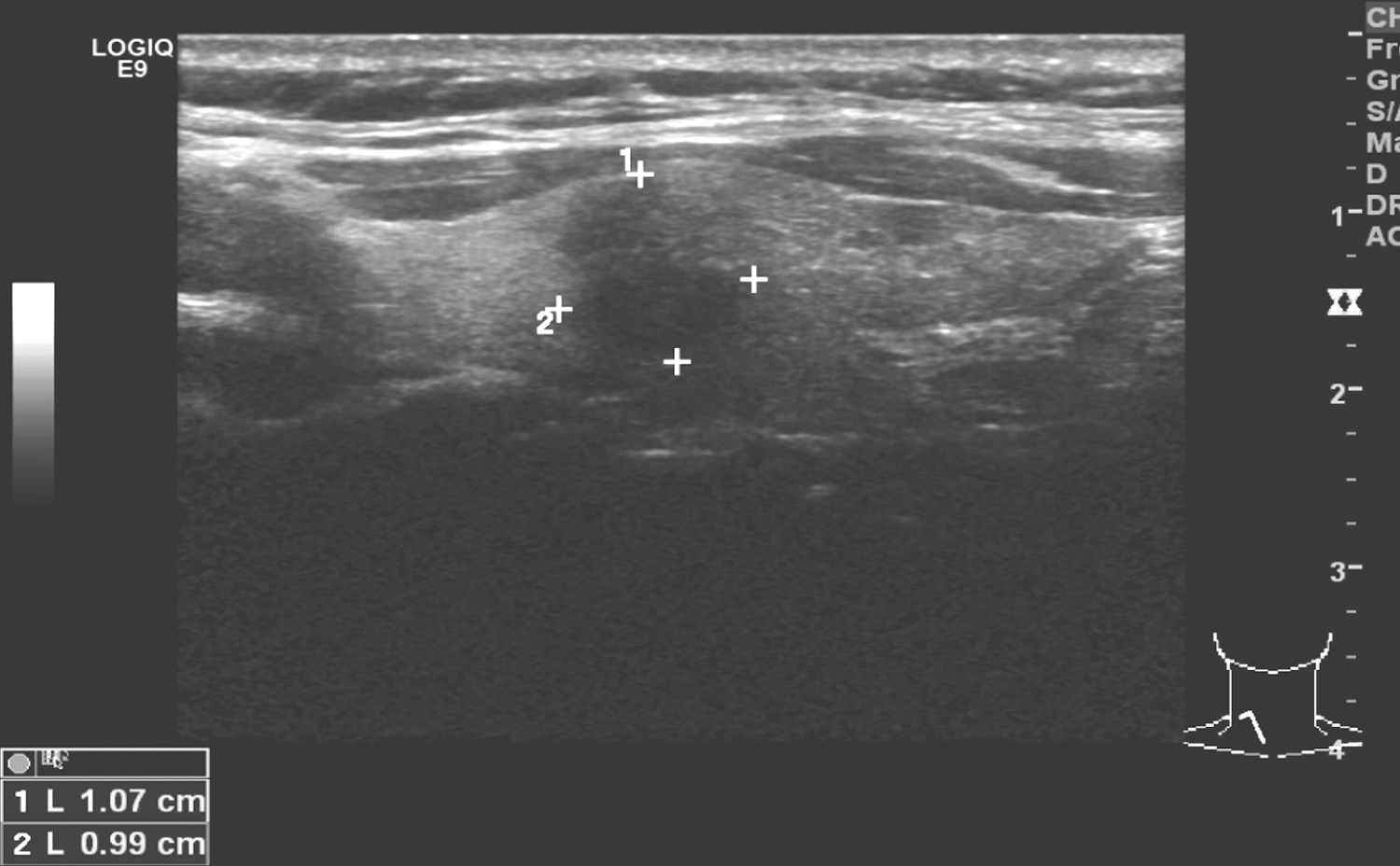
目前影像学检查均提示病变来源于胰腺可能性大。CT考虑实性假乳头状瘤可能,查阅文献发现,实性假乳头状瘤由实性部分和囊性部分混合而成,CT表现取决于二者的比例,特征性表现为“浮云征”(明显强化的实性部分漂浮在低密度的囊性部分中),有时囊性与实性相间分布、不规则排列或存在壁结节。有时肿瘤以实性部分为主。该患者的CT表现与文献表现较符合,但SPT多发于年轻女性,中老年患者较少见。且肿瘤多见于胰头部,胰体尾部及胰腺外较少见,患者临床表现与此不甚符合。为进一步明确诊断,遂行超声内镜检查。EUS提示:胰腺头颈部形态规则,内部回声均匀,胰管无扩张扭曲,于胰腺尾部可见一中等回声、圆形、边界清楚之囊实性团块,以实性成分为主,散在多个大小不等无回声暗区,大小约3.5cm×3.1cm,周围淋巴结无肿大,病变未侵犯周围脏器。诊断为:胰腺囊实性占位(实性假乳头状瘤可能)(见文末彩图3-32-2)。因患者家属表示如有手术机会即考虑手术治疗,未行细针穿刺活检。
患者目前诊断考虑实性假乳头状瘤可能,但仍不甚明确,结合患者临床表现及影像学资料,请外科会诊后认为手术指征明确,与患者家属沟通病情后家属要求手术治疗。遂转入外科行胰体尾切除+脾切除术,术后恢复良好。
图3-32-2 EUS示:胰腺囊实性占位(实性假乳头状瘤可能)
术后病理镜检提示:肿瘤细胞圆形、多角形,体积较小,大小较一致,胞浆少,核深染,排列成实性片状或网状,并可见玻璃样间质及灶性出血。胰腺切缘及脾脏未见肿瘤组织,胰岛细胞多灶性增生。诊断为:(胰)高分化神经内分泌肿瘤(G1)。
免疫组化示: CgA(+); Ki-67(+)。诊断:(胰腺)高分化神经内分泌肿瘤(G1)。
患者病理结果阳性,诊断为胰腺神经内分泌肿瘤,已行外科手术治疗。病理胰腺切缘及脾脏未见肿瘤组织,患者恢复后出院。
最终诊断:胰腺神经内分泌肿瘤。
文献复习:胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumors,PNETs)是来源于胰腺多能神经内分泌干细胞的一类肿瘤,属少见疾病。国外报道其发病率为(1~4)/100万,占所有胰腺肿瘤的2%~3%。与胰腺外分泌肿瘤相比,PNETs进展相对缓慢、手术切除率高、长期存活率高。
对于各种PNETs的分类,从临床表现方面看,根据肿瘤是否分泌具有功能的内分泌激素,将PNETs分为功能性和无功能性两大类。其中,功能性肿瘤占70%~86%,最常见的有胰岛素瘤和胃泌素瘤;较少见的有血管活性肠肽瘤,生长抑素瘤、胰高血糖素瘤、生长激素释放激素分泌肿瘤等;少见的有: PNETs致肾上腺皮质激素瘤、致Cushing综合征、致类癌综合征、致高钙血症等;罕见的有: PNETs异位分泌降钙素、黄体素激素、红细胞生成素、胰岛素样生长因子Ⅱ等。无功能性肿瘤占14%~30%,它们仅分泌胰腺多肽类,较少或不分泌激素,故不产生临床征象。功能性肿瘤由于早期即可产生相应的临床症候群,因此确诊时瘤体多较小,可获得及时治疗。而无功能性肿瘤因缺乏特异性临床表现,多为偶然发现或因占位性病变而引起腹痛、黄疸等症状时就诊发现,因而瘤体多较大。部分病例常延误诊断,肿瘤常生长很大,产生局部侵袭或远处转。在本例中,患者因“左腰背部酸胀感1年余”就诊,主要为肿瘤增大引起的压迫症状,无激素分泌引起临床表现,考虑为无功能性肿瘤。从组织学方面看,WHO给予的分类是:①分化型PNETs,仅显示出一些恶性肿瘤的潜能;②分化型PNE癌,低度恶性;③未分化型PNE癌,高度恶性。
对于神经内分泌肿瘤患者,手术是首选治疗方法。PNETs尽管少见,但很容易发生肝转移,因此术前定位诊断的准确性是决定手术成败和患者预后的关键。它不但可以了解原发性肿瘤的位置、大小以及侵犯范围,指引手术的进行;还可协助制订手术方案,选择手术入路,减少对周围组织器官的损伤以降低并发症发生率;同时还有助于了解转移病灶的情况、了解手术或辅助治疗后病灶的变化等。但到目前为止,PNETs的诊断仍然面临许多困难,主要是该病较为少见,临床症状又缺乏特异性,根据症状难以判断可能的肿瘤类型。B超、CT、MRI、内镜技术等影像学检查对明确肿瘤部位、帮助选择治疗方法具有重要的作用,必要时应行细针穿刺或活检进行病理、特殊染色和相关实验室检查以明确肿瘤类型和分化程度。作为定位诊断方法之一的超声内镜,其在PNETs定位诊断上的重要价值被广泛用于PNETs的定位诊断。EUS可通过胃壁和十二指肠壁近距离对胰腺各部位病变进行超声扫描,还可显示胰周、主动脉周及门静脉周围肿大的淋巴结。可显示的最小病变直径为0.2~0.5cm。提高了PNETs的检率。PNETs的EUS表现具有一定特征性。多数情况下表现为网形或类网形,相对于胰腺实质回声,病变回声明显不同于正常胰腺组织,多呈均匀低回声,边缘与正常胰腺之间界限清晰,边缘多比较完整。少数情况下病变呈中等回声或强回声,还可伴有囊性变,甚至钙化。病灶大、呈等回声、高回声或不均匀回声、侵及血管、伴胰管梗阻或伴周围淋巴结肿大时常提示有恶性病变的可能。但EUS是主观性很强的一项检查,其准确性在很大程度上依赖于检查者的操作技术和临床经验。在本例患者中,EUS检查对病变的部位、大小及周围淋巴结的情况进行了观察,但并未对病变性质予以明确诊断,可能与操作者对此类病变临床经验较少有关。
PNETs唯一可以治愈的方法是完全切除肿瘤。外科手术视肿瘤大小、肿瘤起源位置、肿瘤负荷程度以及患者健康情况来选择和决定具体方案。对于无法切除或发生远处转移的病例,可选择其他治疗模式包括射频消融、化学药物栓塞、碘治疗、其他类型的全身系统治疗、内科药物治疗等。
(郭晓榕)
参考文献
1. Norton JA.Surgery for primary pancreatic neuroendocrine tumors.JGastrointest Surg,2006,10(3): 327-331.
2. Ozao-Choy J,Friedman ML,Kim AS,et al.Radioembolization for treatment of livermetastases from neuroendocrine tumors: correlation with imaging and biomarkers.Pancreas,2013,42(2): 358-360.
3. Heller MT,Shah AB.Imaging of neuroendocrine tumors.Radiol Clin North Am,2011,49(3): 529-548.
4. Anderson MA,Carpenter S,Thompson NW,etal.Endoscopic ultrasound is highly accurate and directsmanagement in patients with neuroendocrine tumors of the pancreas.Am J Gastroenterol,2000,95(9): 2271-2277.
5. Boudreaux JP.Surgery for gastroenteropancreatic neuroendocrine tumors(GEPNETS).Endocrinol Metab Clin North Am,2011,40(1): 163-171.
来源:《消化科病例分析:入门与提高》
作者:辛永宁 柏愚
参编:李兆申 宣世英 李海 尧颖 梁志海
页码:386-389
出版:人民卫生出版社
- 评价此内容




 3我要打分
3我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号

 会员登录
会员登录

