一例侵袭性NK细胞白血病/淋巴瘤的诊疗经验分享
42岁女性,因“反复发热25天”入院 ,曾在当地医院就诊时发现轻度贫血和血小板减少。抗感染治疗后症状反复,遂转诊至一三甲医院,先后经抗感染治疗仍发热, 期间查全身PET-CT,考虑为淋巴瘤,遂转诊至笔者医院。如何诊治?
一、病情摘要
1.基本情况
女性患者,42岁,因“反复发热25天”,于2016年10月入院。25天前,患者无明显诱因出现发热(体温最高达40.8℃)伴头痛、乏力、心悸、畏寒,多于下午及夜间出现,无寒战、咳嗽、咳痰、腹痛、腹泻、尿频、尿急、尿痛、皮疹、关节疼痛、胸闷、胸痛、盗汗,于当地医院就诊时发现轻度贫血和血小板减少。经拉氧头孢、头孢曲松他唑巴坦抗感染治疗,患者症状反复,遂转诊至一三甲医院。实验室检查显示,血常规WBC 4.15×109/L,Hb 90g/L,PLT 58×109/L;C反应蛋白95.3mg/L,降钙素原1.42ng/L;中段尿培养见大肠埃希菌>100000cfu/ml;血培养见凝固酶阴性葡萄球菌;EB病毒DNA 1.74×105/ml。先后经亚胺培南西司他丁、万古霉素、阿昔洛韦、美罗培南等抗感染治疗,患者体温仍在39.5℃左右波动,且出现血压低,需多巴胺维持。期间查全身PET-CT显示脾大伴代谢增高(SUVmax7.7),全身骨髓代谢弥漫增高(SUVmax8.8),考虑为淋巴瘤,遂转诊至我院。
2.既往
2型糖尿病病史。
3.入院查体
体温39.3℃,脉搏108次/分,呼吸20次/分,血压80/60mmHg。神志清楚,全身浅表淋巴结未触及肿大。口唇无发绀,胸廓无畸形。双肺呼吸音对称,未闻啰音。心律齐,P2>A2,各瓣膜听诊区未闻杂音。腹平软,无压痛、反跳痛,肾区无叩痛,肝、脾肋下未触及。
4.入院前检查
(1)实验室检查:
血常规:WBC(4.15~6.20)×109/L,Hb(90~103)g/L,PLT(58~70)×109/L;C反应蛋白95.3mg/L,降钙素原1.42ng/L;肝功能、心功能、肾功能大致正常。
凝血功能:凝血酶原时间16.1s,活化部分凝血酶原时间47.4s,纤维蛋白原1.32g/L,D-二聚体0.62mg/L。
病原检测:病毒抗体阴性;TORCH阴性;半乳甘露聚糖(GM试验)、真菌葡聚糖(G试验)均阴性;EB病毒DNA 1.74×105/ml;巨细胞病毒DNA阴性;中段尿培养见大肠埃希菌>100000cfu/ml(药敏试验提示为敏感菌);血培养见凝固酶阴性葡萄球菌;血涂片未找到疟原虫。自身抗体检查均为阴性。CEA、AFP、CA125、CA199未见异常。
(2)影像学检查:
胸部CT未见肺内活动性病变;腹部B超可见脾厚径48mm,提示脾大。全身PET-CT显示脾大伴代谢增高(SUVmax 7.7),全身骨髓代谢弥漫增高(SUVmax 8.8),考虑为淋巴瘤。
(3)骨髓穿刺检查:
吞噬细胞占1%,巨噬细胞及血小板减少。
(4)骨髓病理:
未见肿瘤细胞。
5.初步诊断
发热待查(疑似噬血细胞综合征),合并葡萄球菌血流感染、泌尿系感染、EB病毒感染。
二、诊治过程
【病例特点】
1.一般情况
患者为中年女性,亚急性病程,有2型糖尿病病史。
2.主要症状和体征
反复发热为主要症状,入院查体仅见血压偏低,未发现其他阳性体征。
3.实验室检查
血常规示轻度贫血及血小板减少,C反应蛋白、降钙素原水平升高,EB病毒DNA 1.74×105/ml;血培养见凝固酶阴性葡萄球菌;中段尿培养见大肠埃希菌>100000cfu/ml;全身PET-CT显示脾及全身骨髓代谢弥漫增高。
4.治疗反应
在外院先后经亚胺培南西司他丁、万古霉素、阿昔洛韦、美罗培南等抗感染治疗,患者仍反复发热,体温在39.5℃左右波动,并出现血压低(需多巴胺维持)。
【鉴别诊断思路】
本例患者为中年女性,急性起病,反复发热,并出现血压偏低、贫血及血小板减少,C反应蛋白、降钙素原增高,首先考虑可能为感染性疾病所致。可能的病因有:①严重细菌感染,尤其菌血症、脓毒血症等可引起发热、血压降低、血细胞减少等。本病例血培养及中段尿培养分别检出葡萄球菌及大肠埃希菌,支持细菌感染诊断。②病毒感染,如EB病毒、巨细胞病毒感染亦可出现高热、血细胞减少。本例患者EB病毒DNA升高,提示存在EB病毒感染。③结核一般起病较缓,临床表现以低热为主,发生血行播散性感染时可出现高热症状。④伤寒、恙虫病、布氏杆菌感染等也可以出现类似临床表现。
患者在外院根据血培养及尿培养药敏试验结果,采取广谱抗感染治疗,但效果不佳。实验室检查显示,疟原虫、肿瘤标记物、真菌、自身免疫抗体均阴性,结合EB病毒DNA升高及全身PET-CT结果,应考虑非感染性疾病,如血液系统疾病(如恶性淋巴瘤)所致发热。另外,患者脾大、血细胞减少,有低纤维蛋白原血症,骨髓穿刺检查可见吞噬细胞,应考虑噬血细胞综合征(hemophagocytic syndrome,HPS)可能。HPS又称噬血细胞性淋巴组织细胞增多症(hemophagocytic lymphohistiocytosis,HLH),成年人发病。对于本病例,需筛除原发性HPS,检测先天性噬血细胞综合征相关基因。
【诊治措施】
1.入院后相关检查
(1)实验室检查
血常规:WBC 6.7×109/L,Hb 74g/L,PLT 10×109/L;血凝全套:凝血酶原时间16.6s,纤维蛋白原1.06g/L,纤维蛋白(原)降解产物9.7μg/ml,D-二聚体4.08mg/L;生化:直接胆红素8.3μmol/L,ALT 41U/L,乳酸脱氢酶147U/L;铁蛋白>1500.0μg/L;CD25>7500U/ml;EB病毒DNA3.52×104/ml。T细胞亚群:CD4/CD8 2.25,NK 3.0%,CD19 25.0%;C反应蛋白8.95mg/L,免疫球蛋白G 8.84g/L,补体C3 0.57g/L,自身免疫指标阴性,结核抗体阴性,T-SPOT阴性;恙虫病、流行性出血热、钩端螺旋体、布氏菌抗体检测阴性。
(2)骨髓涂片
红细胞系增生,巨核-血小板减少,组织细胞可见,偶见吞噬血小板(图1)。
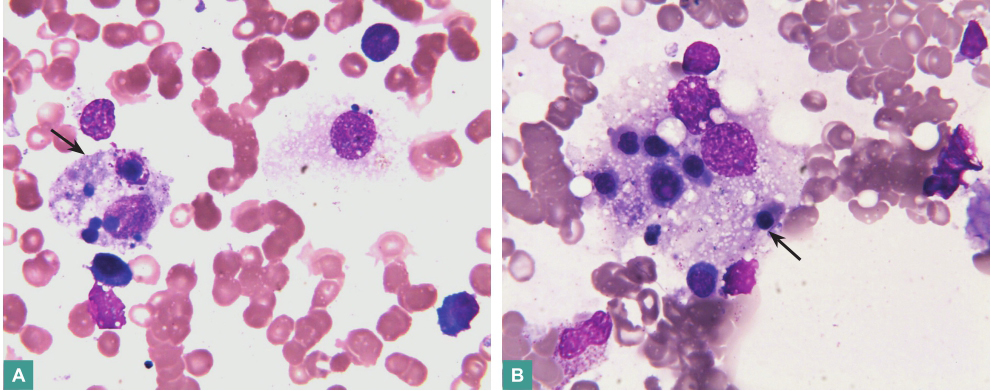
图1 骨髓涂片见吞噬血小板或红细胞的组织细胞(箭头标记)(瑞氏染色,×400)
(3)基因检测
先天性噬血细胞综合征相关基因检测阴性。骨髓T细胞受体(T cell receptor,TCR)、免疫球蛋白重链(immunoglobulin heavy chain,IgH)基因重排阴性。
(4)骨髓活检病理
骨髓增生较活跃,红细胞系比例增高,未见白血病及淋巴瘤证据。
2.入院后相关治疗
入院后继续美罗培南联合万古霉素抗感染方案及去甲肾上腺素、补液等抗休克治疗、输血支持治疗,患者仍发热,加用甲泼尼龙治疗后体温下降,监测血常规显示相关指标进行性下降。
患者反复发热,并出现脾大、血细胞减少、低纤维蛋白原血症、铁蛋白升高,CD25升高,符合噬血细胞综合征表现。全身PET-CT检查见脾脏及骨髓高代谢,两次骨髓穿刺及活检均未见肿瘤依据,先天性噬血细胞综合征相关基因检测阴性,EB病毒DNA升高(因患者血小板低无法行脾组织活检),考虑为EB病毒感染相关性噬血细胞性淋巴组织细胞增多症(HLH)。
采取HLH 2004方案[环孢素(150mg,每12小时1次)、依托泊苷(50mg,d1~d2;100mg,d3~d6、d9~d13)、地塞米松(15mg,d1~d14;10mg,d15~d21;7.5mg,d22起)]治疗后,患者体温恢复正常,无出血倾向。期间,患者出现粒细胞缺乏继发肛周感染,采取粒细胞集落刺激因子促粒细胞生长、抗感染并积极输血等治疗。治疗2周后,在地塞米松减量过程中,患者再次出现反复发热,体温最高达38.9℃,血象仍无改善。
复查骨髓象:
增生活跃,分类不明细胞占13.5%,疑似淋巴瘤细胞侵犯骨髓,伴组织细胞噬血(图2)。
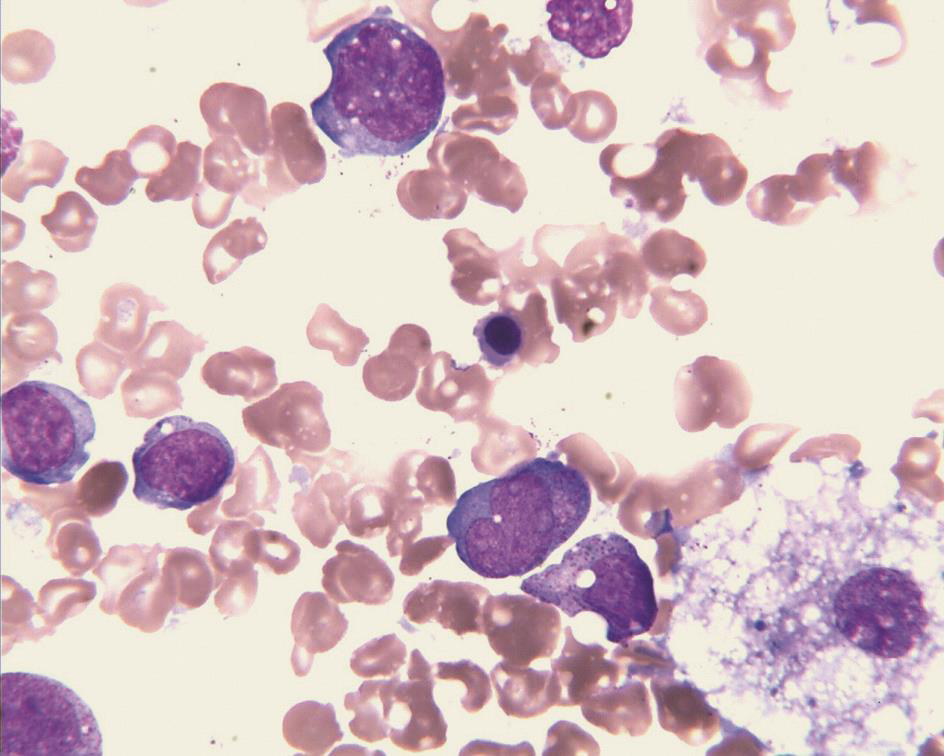
图2 骨髓涂片见分类不明细胞(箭头标记)(瑞氏染色,×400)
流式细胞学:
可见异常NK细胞占7.46%,约占淋巴细胞38.4%,强表达CD45和CD56,表达CD94、GranzymeB、Perforin和CD2,弱表达CD7、CD8,不表达CD16、CD57、CD5、CD3、CD4(图3)。
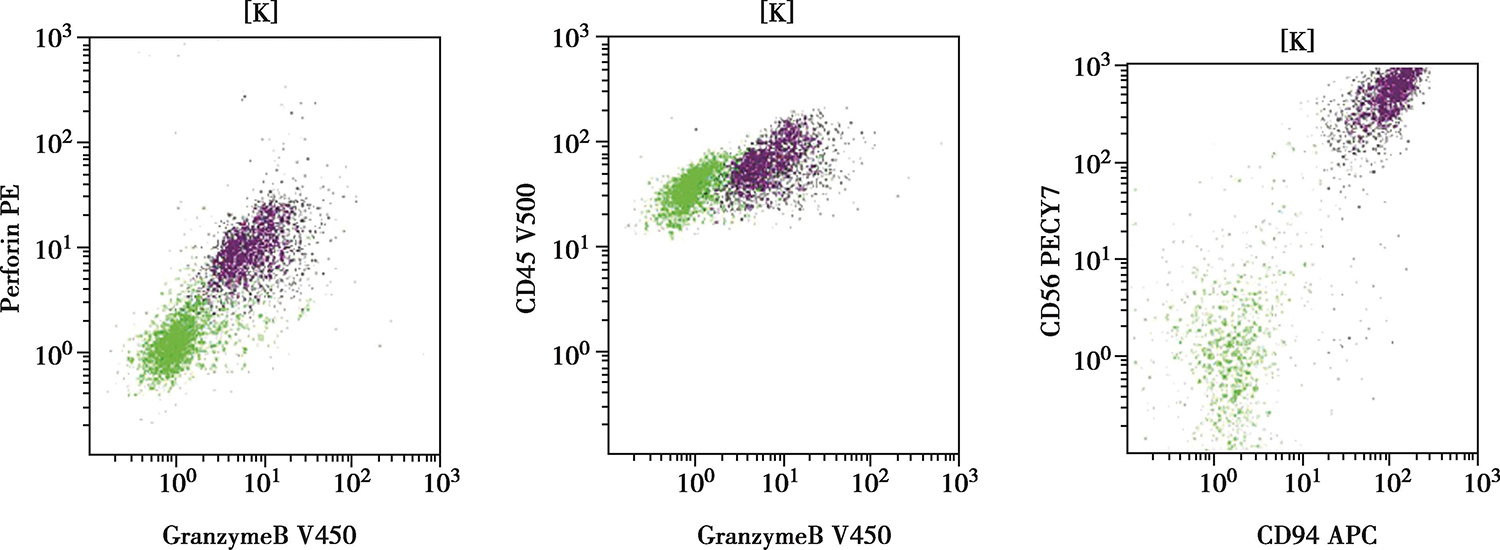
图3 骨髓流式细胞学检查
异常NK细胞强表达CD45、CD56,表达CD94、GranzymeB、Perforin
骨髓活检病理(图4):
骨髓组织细胞增多,免疫组化显示NK细胞增多,胞体偏大,胞质丰富,部分细胞核形态不规则,核仁明显。该类细胞抗原表达如下:PAX5(-)、CD20(-)、CD3ε(+)、CD5(-)、CD2(+)、CD7(-)、CD4(-)、CD8(-)、CD56(+)、CD30(-)。
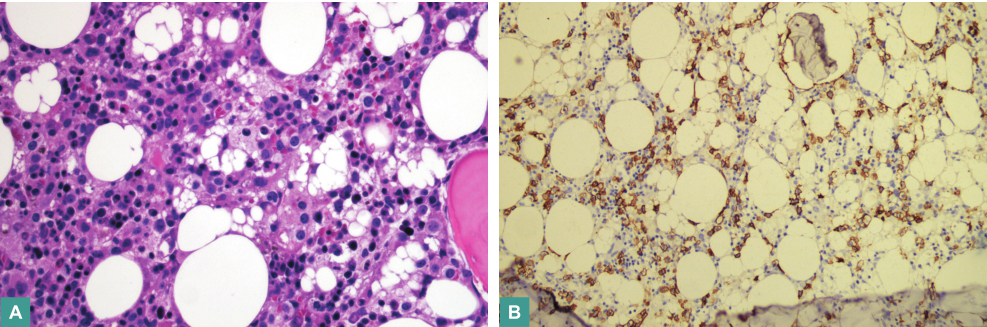
图4 骨髓活检病理
A.组织细胞增多(HE染色,×400);B.免疫组化CD56阳性(×200)
3.最后诊断
侵袭性NK细胞白血病/淋巴瘤。
【临床转归】
采取含培门冬酰胺酶的联合方案(吉西他滨1.4g、奥沙利泊1.4g、培门冬酰胺酶3750U)化疗后,患者出现血压下降,神志模糊、出血倾向,肝肾功能进行性恶化、血凝明显异常,自动出院。
【临床难点】
本例患者以反复发热起病,起病之初出现血压降低,血培养和尿培养阳性,支持细菌感染诊断,但经过广谱抗感染等处理后仍反复发热,并出现全血细胞减少,此后一系列检查结果支持噬血细胞综合征(HPS)诊断。HPS包括原发性和获得性两个类型。原发性HPS发病年龄多在2岁以下,大多伴有常染色体或性染色体隐性遗传。获得性HPS可出现于任何年龄阶段,以8岁以上者多见,常见病因有感染、恶性肿瘤、自身免疫病、药物等。感染相关性HPS多由病毒感染所致,其中以EB病毒感染最为常见。恶性肿瘤相关性HPS多数发生于成年人,以恶性淋巴瘤相关HPS居多。本病例在寻找HPS病因中,相关基因检测显示为阴性,排除原发性HPS,先后2次骨髓穿刺及骨髓活检均未找到肿瘤依据,自身免疫抗体检测阴性,真菌及其他特殊感染检查均阴性,仅EB病毒DNA升高,故考虑为EB病毒感染相关性HLH。采取HLH-2004方案治疗后,患者体温一度正常,但在治疗过程中再次出现高热。距起病50天,经第3次骨髓穿刺活检才明确诊断侵袭性NK细胞白血病/淋巴瘤(aggressive NK cell leukemia,ANKL)。
三、点睛析评
本病例以反复发热为主要症状,并出现全血细胞减少伴脾大,广谱抗感染治疗效果不佳,相关检查支持HLH诊断,按HLH治疗一度体温恢复正常,第3次骨髓穿刺活检明确诊断为侵袭性NK细胞白血病/淋巴瘤。
2005年,美国血液病协会推荐HLH的诊断标准为:分子生物学诊断符合HPS或符合以下8条指标中的5条即可诊断:①发热:持续>7天,体温>38.5℃;②脾大(肋缘下>3cm);③血细胞减少(外周血三系中至少有两系减少):血红蛋白<90g/L(<4周婴儿:血红蛋白<100g/L),血小板计数<100×109/L,中性粒细胞计数<1.0×109/L且非骨髓造血功能减低所致;④高甘油三酯血症和(或)低纤维蛋白原血症:空腹甘油三酯≥3.0mmol/L,纤维蛋白原≤1.5g/L;⑤骨髓、脾或淋巴结中发现噬血现象;⑥NK细胞活性减低或缺失;⑦铁蛋白≥500μg/L;⑧可溶性IL-2受体(sCD25)水平明显升高。对于HPS的治疗主要依据HLH-2004治疗方案,基本方案为依托泊苷+地塞米松+环孢素,同时针对原发病治疗。
ANKL是2008年WHO淋巴组织肿瘤分类中的一个独立类型,发病率低,主要见于青少年和壮年,病死率高,中位生存期仅2个月,目前尚无有效治疗方法,普通化疗完全缓解率在20%以下。目前ANKL在国内外均为散发报道,目前国外文献资料中普遍使用的诊断标准:①发热、消瘦、盗汗等症状明显,多伴有肝、脾大,淋巴结及胃肠道受累;②可伴有全血细胞减少;③外周血、骨髓或病理活检组织中见克隆性增殖的NK细胞型大颗粒淋巴细胞,细胞免疫表型为:CD2阳性、sCD3阴性、胞质CD3阳性、CD56阳性、CD57阴性,CD1lb和CD16可以阳性,无TCR、IgH基因重排;④有EB病毒感染的实验室证据;⑤无特异性染色体异常,核型异常多为del(6)(q21q25);⑥排除引起大颗粒淋巴细胞增多的其他疾病。NK细胞具有对多种化疗药物耐药的p糖蛋白,故淋巴瘤常规CHOP治疗方案对本病无效。近年的研究证实,甲氨蝶呤及左旋门冬酰胺酶、培门冬酰胺酶有抗NK细胞肿瘤活性,病情一旦缓解,应尽快行异基因骨髓移植。
知识来源
人卫知识数字服务体系
- 评价此内容




 3我要打分
3我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号

 会员登录
会员登录

