一食管鳞癌患者新辅助放疗中情况不断 围术期该注意什么?
新辅助放疗使某些肿瘤得以基本控制或症状减轻、癌瘤缩小,从而使手术机会明显增加。尤其在一些局部晚期肿瘤患者中,如食管癌、直肠癌和宫颈癌等,术前新辅助放疗已被广泛应用,可增加手术切除机会、减少局部复发率并延长生存率。但术前新辅助放疗特别是长时间、多疗程的放疗对各脏器的毒性作用,如心肺毒性、肝肾毒性等等,可能会给麻醉手术带来一定的危险性。因此,术前新辅助放疗的肿瘤病人施行麻醉手术时,围术期的安危已逐步引起了麻醉医师的重视,麻醉医师需要对放疗相关毒副作用及防治措施有必要的了解,术前与相关科室医师合作评估患者各系统情况,共同把握好麻醉、手术时机,做好肿瘤患者的围术期管理,利于患者术后快速康复(ERAS)。
【病例简介】
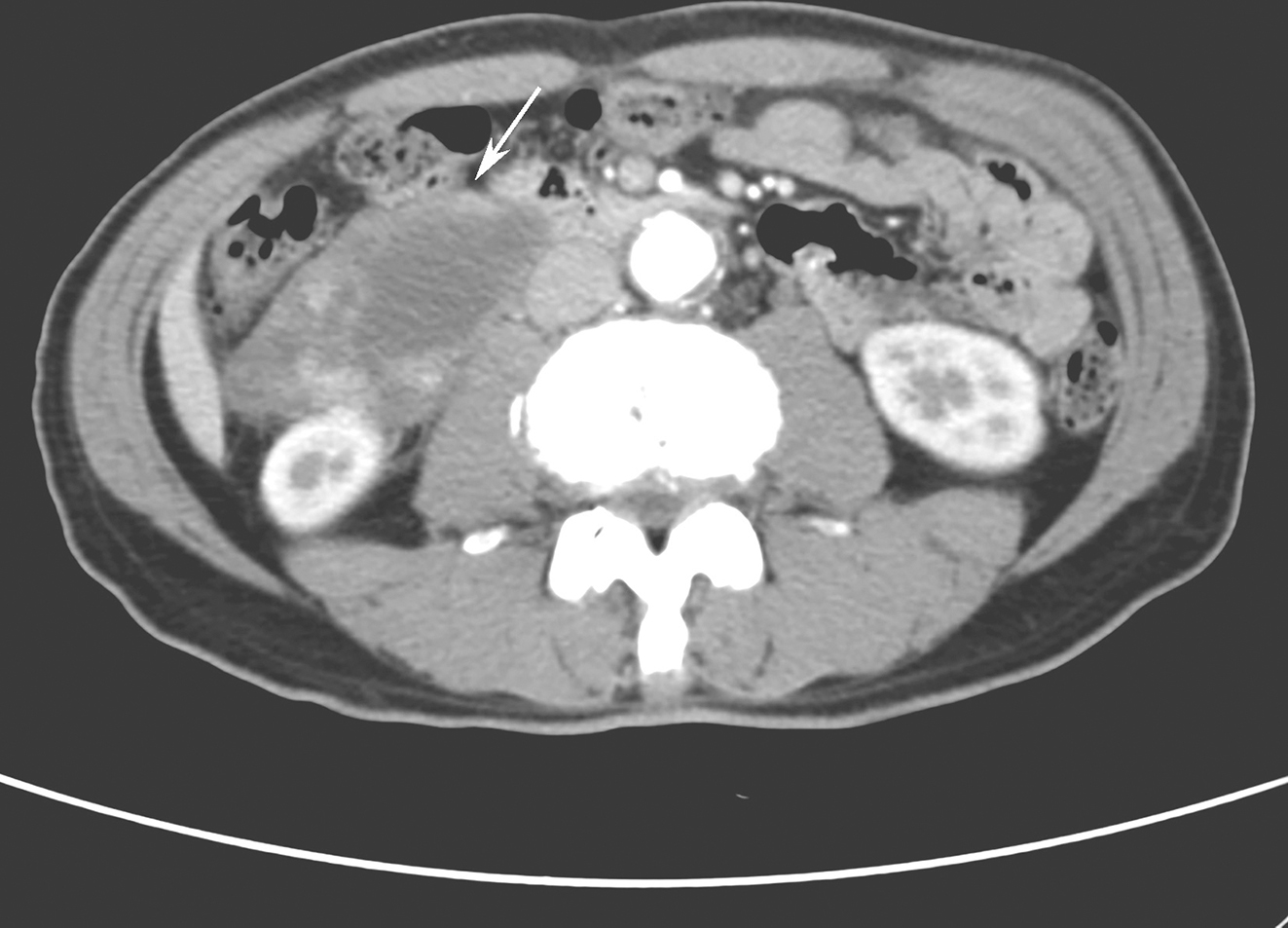
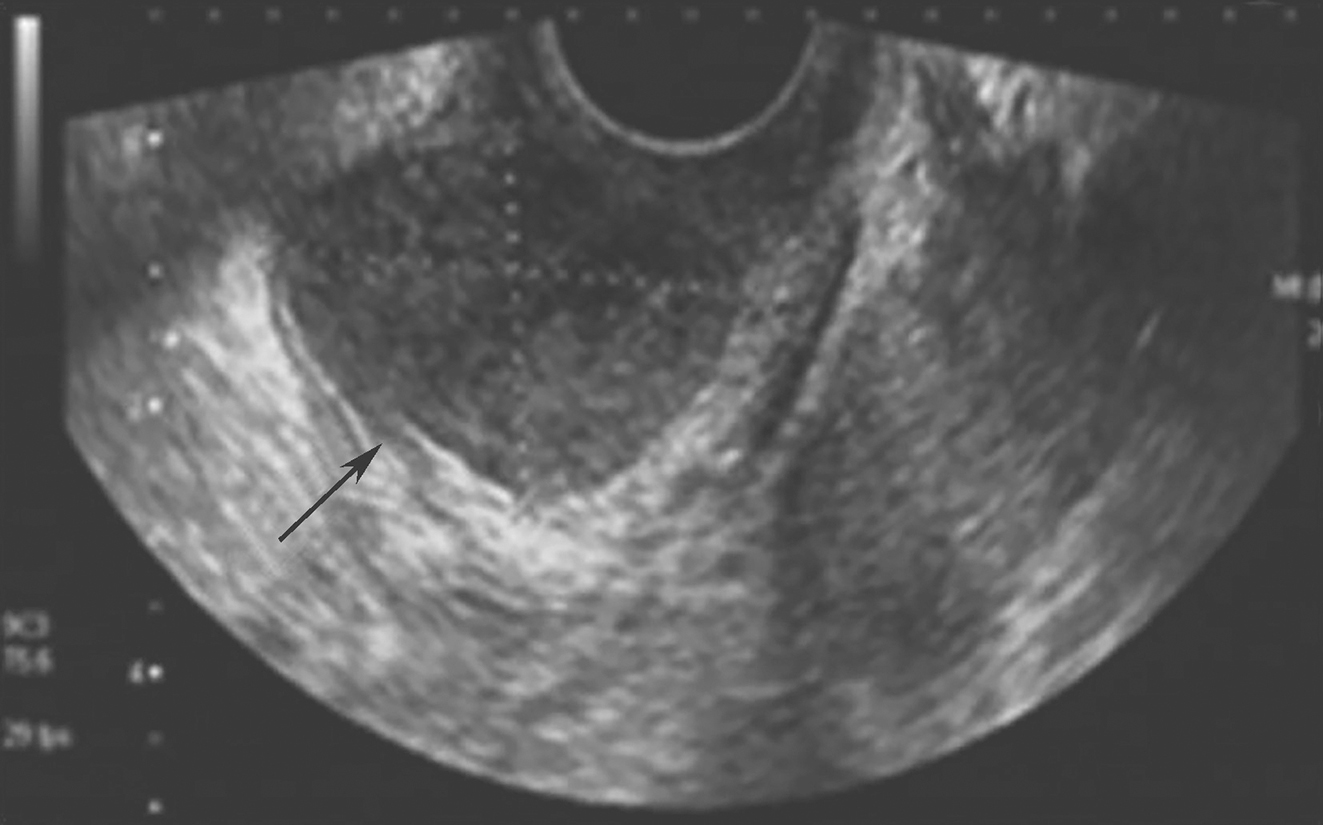
患者,男性,60岁,71kg。于入院前2个月出现吞咽困难伴胸骨后不适,无呕吐、呃逆、声嘶、黑便、骨关节疼痛等症状,无高血压、心脏病史,术前心电图正常。胃镜检查发现距切牙30~35cm见食管绕壁浸润生长的菜花样肿物,病理诊断为食管低分化鳞状细胞癌;胸部CT提示食管中段癌并纵隔淋巴结转移,两侧腋窝淋巴结转移?临床诊断为胸中段食管鳞癌,纵隔多发淋巴结肿大。胸瘤外科考虑手术难度大,决定先行食管癌术前新辅助放疗,处方剂量为PGTV,PGTV-nd 44.1Gy/21f,PCTV 42Gy/21f。患者在放疗过程中全身多处皮肤瘙痒,考虑放射线过敏所致,给予扑尔敏抗过敏处理好转;出现顽固性呃逆,考虑为食管癌梗阻、肿瘤压迫膈神经引起,予托烷司琼及地塞米松对症止吐治疗后缓解;放疗后出现窦性心动过速,考虑放疗引起的相关心脏毒副作用,暂给予观察。复查胸部CT提示肿瘤消退达到部分缓解(PR)状态。患者休息3周后在全麻下行经右胸、上腹、右颈三切口食管癌根治术+胸膜粘连烙断+胸腔闭式引流术。术前检查:白蛋白29.4g/L,前白蛋白74mg/L,餐后2小时血糖8.1mmol/L,D-Dimer(DD)4.78mg/L;心电图提示窦性心动过速,余检查未见特殊。
全麻诱导及维持均采用丙泊酚(靶控输注,TCl)、瑞芬太尼TCl,顺式阿曲库铵间断推注,手术时间约6小时,出血量约550ml,尿量450ml,共补液2500ml,其中晶体1500ml,胶体1000ml,输血浆200ml。麻醉期间心率较快,循环、呼吸稳定,术后转入恢复室(PACU),顺利拔管。术后第1天患者血压稳定,心率约125次/分,予西地兰强心治疗。术后16天经口进食未见异常,术后20天顺利出院。
【问题】
1.肿瘤患者术前新辅助放疗的适应证?
放疗一般包括根治性放疗、姑息性放疗以及与手术和化疗相结合的综合治疗。放疗适应证很广,70%以上的肿瘤患者需要接受放疗,50%左右可达根治性效果。放疗除用于恶性肿瘤外,还可用于治疗一些良性肿瘤,如垂体病、血管瘤、腮腺混合瘤、顽固性神经性皮炎、瘢痕疙瘩等多种良性疾病。当肿瘤较局限,或只有邻近组织侵犯或淋巴结转移,且肿瘤对射线又较敏感时,根治性放疗可作为主要治疗手段,如鼻咽癌等头颈部肿瘤、肺癌、食管癌、淋巴系统恶性肿瘤、前列腺癌、宫颈癌等。而术前新辅助放疗可提高肿瘤的切除率,减少术中肿瘤种植机会及术后复发率,一般适用于食管癌、喉癌、上颌窦癌、软组织肉瘤、直肠癌等。
食管癌容易侵犯周围的大血管、气管、支气管等组织,也容易发生淋巴结转移,而远处淋巴结较大等,单纯手术治疗效果较差,手术切除率较低。因此,术前新辅助放疗能有效减小肿块体积,减轻肿瘤对周围组织的浸润,降低局部复发率,提高手术疗效。此病例患者术前检查提示食管癌伴纵隔多发淋巴结转移,与周围组织关系密切,外科医生考虑根治性手术清除较难,有进行术前新辅助放疗指征。经放疗后,食管肿物明显缩小,纵隔淋巴结较前缩小约50%,放疗后评估达PR状态,可进行下一步手术治疗。
2.常用的放疗方法有哪些?
放疗一般有体内照射和体外照射两种。
体内照射又称为近距离放射治疗,是把高强度的微形放射源直接插入肿瘤组织内(如皮肤癌、舌癌等)、器官内腔(如食管、宫颈等)进行照射,疗效肯定,而正常组织不受过量照射,以避免严重并发症发生。
体外照射是放疗的主要方法,常用的有:二维放疗、三维适形放疗(3DCRT)、调强适形放疗(lMRT)、图像引导放疗(lGRT)、容积旋转调强放疗(VMAT)、螺旋断层放疗、质子放射治疗等。三维适形放疗为使用多波束和构建剂量体积直方图来评估分布在肿瘤和正常结构的剂量(特别是食管、心脏、肺和脊髓等器官剂量)。调强适形放疗为类似维适形放疗,通过多波束治疗,可在治疗中改变放射线的影响和逆向调强治疗(即在设计治疗射束前就限定好正常组织的受量)。容积旋转调强放疗是在图像引导放疗基础上发展而来,其以旋转照射的动态容积lMRT技术为基础,与lMRT相比较,高效、快捷、准确,在靶区剂量分布方面优势明显。螺旋断层放疗是一种先进的调强放疗方式,对中下段食管癌放疗可提高靶区剂量均匀性、适形度。此病例患者采用了现常用的三维适形放疗。3DCRT可以使高剂量分布区与靶区保持高度一致,可以让肿瘤靶区接受到足够的照射剂量的同时降低周围正常组织接受量,患者食管癌与气道及纵隔淋巴结与心肺关系密切,使用此放疗方法可达到治疗效果并减少心肺相关毒性。
3.放疗常见的毒副作用及防治措施?
放疗毒副作用分为急性毒副作用(即时反应)和慢性毒副作用(延迟性反应)两类。急性毒副作用是在放疗期间出现的反应,可因人、因放疗部位而异。慢性毒副作用是指放疗后数周甚至数年才出现的反应,包括早发性延迟反应和晚发性延迟反应。早发性延迟反应一般在放疗后数周至3个月左右出现,如放射性肺炎、中枢神经系统放疗后3~4个月内出现头晕、嗜睡、脑脊液中白细胞增多等中枢神经症状和体征;晚发性延迟反应一般在放疗后数月至数年出现,如放射性脊髓炎、放射性骨炎、骨坏死等。
常见的毒副作用有:
(1)皮肤和肌肉损伤:
是常见的毒副作用。皮肤对射线的耐受量与所用放射源、照射面积和部位有关,皮肤损害根据严重程度分为Ⅰ度反应、Ⅱ度反应和Ⅲ度反应。照射局部从充血、红斑到肿胀、糜烂、溃疡甚至形成窦道,放疗后纤维病变、萎缩及皮肤花斑样改变和色素沉着;局部软组织红肿、疼痛、水肿、蜂窝织炎、坏死、肌肉萎缩、肌痉挛、软组织纤维变、活动受限等。如头颈部照射后颞颌关节受损、张口困难等,加上颈部活动受限和咽喉结构改变而易致全麻气管插管困难。
(2)全身反应:
由于放疗后肿瘤组织崩解、毒素被吸收,在照射数小时或1~2天后,易致乏力、食欲下降、恶心、呕吐等。
(3)造血系统反应:
由于骨髓和淋巴组织对放射线高度敏感,放疗后白细胞下降最明显,其次是淋巴细胞和血小板,红细胞则不敏感。血象反应的差异与照射范围的大小,脾区、骨髓是否被照射,放疗前和放疗中是否应用化疗药物等因素有一定关系。
(4)心肺、食管损伤:
胸部照射时,易致心肺、食管损伤。发生放射性气管炎、放射性肺炎、肺纤维病变。肺功能损害的患者常出现咳嗽、咯血、高热、胸痛、呼吸困难等症状,严重者出现气管狭窄、气管瘘等。放射性肺炎分急性和慢性,急性者常发生在放疗后1~6个月,与照射面积有关;慢性者主要因肺纤维病变导致,常于放疗后2~3个月再现,可持续多年。心脏损伤主要表现有心律失常、心包炎、心包积液、心肌炎、心肌梗死等。据报道心脏体积1/3受照时照射剂量为70Gy,2/3体积受照射时55Gy,全脏受照射时50Gy,心脏损伤发生率明显增高。接受放疗的纵隔恶性肿瘤患者中,心包积液的发生率高达30%,但多数患者临床症状不明显,可自行缓解,仅11%有症状。食管损伤主要有放射性食管炎、食管穿孔、食管气管瘘、食管出血等,据报道放疗后食管气管瘘的发生率约为6.89%,给麻醉造成困难,术后易窒息、感染甚至呼吸衰竭。
(5)神经系统损伤:
放疗易致神经系统损伤,从放疗开始到神经组织发生凝固性坏死。患者在1~6个月出现程度不同的放射反应,1年后基本消失。神经系统损伤分急性期、亚急性期和慢性期,急性期出现于放疗后4周内,主要症状是恶心、呕吐、癫痫发作;亚急性期发生于放疗后4周~6个月,主要症状是头痛、恶心、记忆力下降、脱发等;慢性期发生于放疗后6个月以上,此期临床表现主要与照射部位有关。在放疗中如忽略了对脊髓的有效保护措施,有可能导致脊髓放射性损伤(放射性脊髓炎),多发生于放疗后数月至数年内,分为早期和晚期、暂时性和永久性,开始表现为渐进性、上行性感觉减退,行走或持重乏力,低头时如触电感,逐渐发展为四肢运动障碍、反射亢进、痉挛甚至瘫痪。
(6)泌尿系统损伤:
肾脏对照射的耐受量较低,据报道常规全肾照射20Gy,5年内有1%~5%的患者发生放射性肾炎,而全肾照射25Gy有50%的患者发生放射性肾炎。急性放射性肾炎常在放疗后6~8周发生,出现蛋白尿、高血压、贫血和心脏肥大等症状体征。在进行盆腔放疗时,约50%~60%的患者在3~4周内发生急性膀胱炎,6个月~2年间可发生亚急性膀胱炎和慢性膀胱炎。
(7)肿瘤远处转移:
可于放疗期间或治疗后出现,术前放疗可能影响术后恢复及增加术后并发症风险等。
防治措施:根据病情、照射部位、疗程等进行综合防治。
(1)保持皮肤的干净和干燥,在照射野禁用刺激性物品,必要时在放疗区皮肤上涂抹保护剂;适当少量激素和抗生素治疗等。
(2)每周检查血象1次,当白细胞下降至3×109/L或中性粒细胞下降至1.5×109/L下时,需给予G-CSF或GSF类升白药物,皮下注射1次/天×3天;如血象下降明显,则暂停放疗。
(3)严密监测血氧饱和度,肺部体征,发现患者血氧饱和度下降、呼吸道分泌物增多时,即应常规吸痰、供氧、气道湿化,使分泌物易排出等;常规给予保护心肌药物,可降低心律失常的发生率。
随着lMRT、lGRT、VMAT、质子放疗等精准放疗技术的不断发展,精确放疗对正常组织的损伤较前明显减少,患者放疗毒副作用较常规放疗明显降低,提高了生活质量和术前机体功能储备。
放疗过程中患者出现放射线过敏及窦性心动过速心脏毒性表现,经过抗过敏处理得到缓解,考虑纵隔靶区放疗时对有心脏一定毒性作用,导致窦性心动过速,但未出现严重心律失常,血流动力学稳定,暂给予继续观察。
4.术前新辅助放疗肿瘤患者围术期管理?
肿瘤患者接受新辅助放疗后,要常规进行相关检查和评估,如肿瘤较前缩小,可考虑择期手术切除。要完善相关术前准备,加强术前综合防治措施,使新辅助放疗后的相关毒副作用得到妥善处理,心肺功能得到进一步改善,麻醉手术耐受力明显提高。
(1)术前准备要注意的几个重要问题。
充分注意肿瘤病人的具体情况采取一些特殊的准备措施。由于放疗不可避免地会对正常组织造成一定的毒副作用,如果肿瘤病人已接受过联合治疗方案,则可造成临床和亚临床的复合性损害。如在放疗之前病人已接受了化疗或手术治疗等,放疗范围内的组织对照射耐受性下降。因此,麻醉医师要特别注意新辅助放疗的方式、部位、剂量、疗程、毒副作用及其防治措施,末次放疗距麻醉手术天数。麻醉选择应注意术前新辅助放疗并发症的问题。腰部放疗或局部受照射的,硬膜外、腰麻相对禁忌,因放疗后皮肤受损、组织反应、水肿、粘连,穿刺时易出血,也增加置管难度。颌面、颈部放疗的患者,术前特别要检查颞颌关节的功能、口咽、鼻咽及张口情况,如发现异常(张口困难、黏膜受损等),则对麻醉都有可能造成严重威胁,易致插管困难、呼吸道阻塞、窒息、感染、出血等危险,术前要及时处理。对放射性肺炎要及时处理,必须戒烟,可用激素、氯喹等纤维母细胞抑制剂,也可吸入低浓度氧气,以减轻肺部病变、改善呼吸功能。术前应特别注意心血管系统的详细检查,加强术前综合治疗,及时纠正心血管并发症,强化心血管功能的保护,以防止麻醉和手术加重心脏的不良反应。如有骨髓抑制情况和出、凝血功能障碍,应予以纠正,以免增加麻醉、手术出血的危险性。
(2)麻醉、手术时机的把握。
术前新辅助放疗后要及时进行相关检查,提示肿瘤消退达到PR状态时可考虑行手术治疗。放疗后应每周检查血常规1~2次,使血象恢复至正常范围,且体质恢复正常时方可手术。一般来说,麻醉、手术应在术前新辅助放疗结束后2~4周施行较为合适,可防止和减少因放疗后心肺损伤导致手术后的早期低氧血症、血流动力学紊乱。对术前有心肺合并疾病的患者,应使心肺功能达到手术标准后方可手术。
(3)围术期管理要点。
围术期注意监测血气分析、肺部体征,减少分泌物,特别是术前合并肺部疾病患者,防止围术期低氧血症及呼吸衰竭等的发生。术前有心电图异常者,术中严密监测心电图变化。尽可能操作轻柔、缩短手术时间,尽量避免对心脏和主动脉过分挤压,术中充分止血,避免多脏器切除。围术期注意维持水电解质平衡,保持血流动力学平稳,避免血压过低,保证冠状血管、脑、肝、肾的灌注量等。术后对合并疾病进行严密监测,及时采用有效措施可减少和纠正早期相关并发症的发生。
放疗过程中患者发生过敏现象,可能存在气道高反应状态,应积极抗过敏治疗,避免在气道高反应阶段进行麻醉,可能诱发气管痉挛,增加麻醉风险。患者存在一定程度心脏毒性,主要表现为窦性心动过速,无明显血流动力学变化,术前准备无特殊处理,术中应注意麻醉药物对循环的抑制作用,进行有创血压监测,维持血压在基础值+20%或-20%,密切观察心电图,积极纠正水电解质紊乱,防止严重心律失常发生,术后6小时、12小时进行心肌酶学监测。手术部位与心脏、纵隔内大血管关系密切,术中进行操作时可能挤压到心脏及上腔静脉,注意严重心律失常、低血压的发生,必要时要求外科医生暂停手术操作,待循环稳定后再进行。监测中心静脉压,避免心脏前负荷加重,防止进一步发生心功能不全。围术期评估肺功能、血气分析、肺部体征,防止术后低氧血症的发生。
【小结】
麻醉医师经常为曾接受过或正在接受放疗的肿瘤患者施行各种麻醉,由于放疗不可避免地会对正常组织造成一定的损害,如果肿瘤患者已接受过联合治疗方案,放疗范围内的组织对照射的耐受性下降,可造成临床和亚临床的复合性损害。因此,肿瘤患者新辅助放疗后施行麻醉处理有其特殊性,要特别注意新辅助放疗的方式、部位、剂量、疗程、毒副作用及其防治措施,末次放疗距麻醉手术天数,结合肿瘤外科特点进行充分的术前准备非常重要。因此,麻醉医师应严密监测围术期血气分析、心电图,维持呼吸、循环功能的稳定,减少相关并发症的发生率。
【专家点评】
何并文,广西医科大学副校长,附属肿瘤医院麻醉科主任医师、教授,医学博士。
1.肿瘤病人当实施综合治疗,放疗是常用的手段之一。传统的放疗是在手术后实施,在术前进行的放疗为新辅助放疗。肿瘤供血充足,含氧丰富,对新辅助放疗更加敏感,且不良反应较传统放疗低,易于耐受,因此,可通过使肿瘤缩小增加手术切除的机会。食管癌单纯手术治疗效果较差,手术切除率较低。因此,术前新辅助放疗能有效减小肿块体积,减轻肿瘤对周围组织的浸润,降低局部复发率,提高手术疗效。
2.放疗因照射的方法、部位、剂量不同,所引起的并发症种类较多。麻醉科医生应建立放疗可引起全身并发症的概念,并结合具体患者实施有针对性的评估。
3.了解新辅助放疗的基本方法和原则,并熟知其相应的不良反应,尤其是重要脏器和气道的影响,对于术前评估非常重要。本例患者在放疗过程中出现了心脏、皮肤受累,引起相应反应。
4.麻醉、手术应在术前新辅助放疗结束后2~4周施行较为合适,可防止和减少因放疗后心肺损伤导致手术后的早期低氧血症、血流动力学紊乱。
5.围术期特别强调对呼吸和循环系统的监测与支持,减少围术期低氧血症的发生,避免血压过低,保证冠状血管、脑、肝、肾的灌注量等。
【参考文献】
1.傅剑华,杨弘.食管癌术前新辅助治疗原则及循证医学依据.中国癌症杂志,2011,21(7):518-521.
2.黄智昊,钟陆行.食管癌放疗技术及放疗方式研究进展.中国肿瘤临床,2016,43(12):527-530.
3.赫捷,中国抗癌协会食管癌专业委员会.食管癌规范化诊治指南.第2版.北京:中国协和医科大学出版社,2013.
4.刘玉中.肿瘤的放射治疗与麻醉//李锦成,王大柱.肿瘤外科麻醉.天津:天津科学技术出版社,2006:122-127.
5.何并文.放疗或化疗肿瘤患者的椎管内麻醉//谭冠先,郭曲练,黄文起.椎管内麻醉学.北京:人民卫生出版社,2011:501-517.
6.Koide Y,Kodaira T,Tachibana H,et al.Clinical outcome of definitive radiation therapy for superficial esophageal cancer.Jpn J Clin Oncol 2017;1-8.DOl:10.1093/jjco/hyx021.
7.Franco P,Arcadipane F,Strignano P,et al.Pre-operative treatments for adenocarcinoma of the lower oesophagus and gastro-oesophageal junction:a review of the current evidence from randomized trials.Med Oncol,2017;34:40.DOl:10.1007/s12032-017-0898-1.
8.Lin SH,Wang L,Myles B,et al.Propensity score-based comparison of long-term outcomes with 3-dimensional comformal radiotherapy vs intensity-modulated radiotherapy for esophageal cancer.lnt J Radiat Oncol Biol Phys,2012,84(5):1078-1085.
9.Patil SS,May KS,Hackett RA,et al.A comparison of VMAT,lMRT,and 3D-CRT in the treatment planning of patients with distal esophageal cancer.Radiat Oncol,2011,81(2):324-325.
(环球医学编辑:常路)
来源:《临床麻醉学病例解析》
作者:王英伟 李天佐
页码:168-172
出版:人民卫生出版社
- 评价此内容




 3我要打分
3我要打分
近期推荐
热门关键词
最新会议
- 2013循证医学和实效研究方法学研讨会
- 欧洲心脏病学会年会
- 世界帕金森病和相关疾病2013年会议
- 英国介入放射学学会2013年第25届年会
- 美国血液学会2013年年会
- 美国癫痫学会2013年第67届年会
- 肥胖学会 2013年年会
- 2013年第9届欧洲抗体会议
- 国际精神病学协会 2013年会议
- 妇科肿瘤2013年第18届大会
- 国际创伤压力研究学会2013年第29届…
- 2013年第4届亚太地区骨质疏松症会议
- 皮肤病协会国际2013年会议
- 世界糖尿病2013年大会
- 2013年国际成瘾性药年会
- 彭晓霞---诊断试验的Meta分析
- 武姗姗---累积Meta分析和TSA分析
- 孙凤---Network Meta分析
- 杨智荣---Cochrane综述实战经验分享
- 杨祖耀---疾病频率资料的Meta分析
合作伙伴
Copyright g-medon.com All Rights Reserved 环球医学资讯 未经授权请勿转载!
网络实名:环球医学:京ICP备08004413号-2
关于我们|
我们的服务|版权及责任声明|联系我们
互联网药品信息服务资格证书(京)-经营性-2017-0027
互联网医疗保健信息服务复核同意书 京卫计网审[2015]第0344号


 会员登录
会员登录

